题目内容
8.纳米CdSe(硒化镉)可用作光学材料.在一定条件下,由Na2SO3和Se反应生成Na2SeSO3(硒代硫酸钠);再由CdCl2形成的配合物与Na2SeSO3反应制得CdSe纳米颗粒.流程图如下: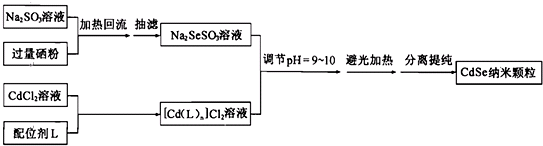
已知:①纳米颗粒通常指平均粒径为1~100nm的粒子
②CdSe纳米颗粒的大小影响会其发光性质.在一定配位剂浓度下,避光加热步骤中反应时间和温度对纳米颗粒平均粒径的影响,结果如图1所示;某温度下配位剂浓度对纳米颗粒平均粒径的影响,如图2所示:

则下列说法中正确的是( )
| A. | 在分离提纯CdSe时一般向溶液中加入丙酮,以增强溶剂极性,有利于CeSe的沉淀,提高收率 | |
| B. | 一般可用NaOH调节Na2SeSO3溶液的pH值,在此过程中会有HSe-和HSO3-生成 | |
| C. | 该纳米颗粒不能使用常压过滤或者减压过滤分离,因为其易在滤纸表面形成一层致密而厚实的膜,阻碍溶剂的通过 | |
| D. | 改变反应温度和反应时间,可以得到不同发光性质的CdSe纳米颗粒;且若要在60℃得到3.0 nm的CdSe纳米颗粒,可尝试降低配位剂浓度的方法 |
分析 A.CdSe是强极性物质,在水溶液中加入丙酮是为了降低溶剂极性;
B.硒代硫酸钠中硒为-2价,硫为+6价,加入NaOH时发生复分解反应;
C.常压或减压时,纳米颗粒能透过滤纸;
D.根据图1知,反应温度和反应时间影响不同发光性质的CdSe纳米颗粒的获取;根据图2知,在一定温度下,获取一定颗粒直径的成分多少与配位剂浓度有关.
解答 解:A.CdSe是强极性物质,在水溶液中加入丙酮是为了降低溶剂极性,利于CdSe析出,故A错误;
B.硒代硫酸钠中硒为-2价,硫为+6价,故加入氢氧化钠后有HSe-和SO42-生成,故B错误;
C.常压或减压时,纳米颗粒能透过滤纸,所以不能使用常压或减压过滤的原因是纳米颗粒易透过滤纸,故C错误;
D.根据图1知,反应温度和反应时间影响不同发光性质的CdSe纳米颗粒的获取,所以改变反应温度和反应时间,可以得到不同发光性质的CdSe纳米颗粒;根据图2知,在一定温度下,获取一定颗粒直径的成分多少与配位剂浓度有关,所以若要在60℃得到3.0 nm的CdSe纳米颗粒,可尝试降低配位剂浓度的方法,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,A项考察对晶体析出条件的掌握和物质极性的判断、B项考察学生对元素化合价的判断和从硫代硫酸钠而来的化合价类推能力、C项考察学生对滤纸过滤原理的考察、D项要求学生具有较强的读图、比较能力,明确实验原理及物质性质、图象分析是解本题关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.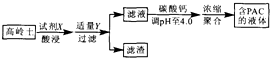 采用高岭土(主要成分为A12 O3、SiO2和Fe2O3)为原料制备水质净化剂PAC{[A12(OH)nC16-n]m(n<6,m为聚合度)}的过程如图.下列说法正确的是( )
采用高岭土(主要成分为A12 O3、SiO2和Fe2O3)为原料制备水质净化剂PAC{[A12(OH)nC16-n]m(n<6,m为聚合度)}的过程如图.下列说法正确的是( )
 采用高岭土(主要成分为A12 O3、SiO2和Fe2O3)为原料制备水质净化剂PAC{[A12(OH)nC16-n]m(n<6,m为聚合度)}的过程如图.下列说法正确的是( )
采用高岭土(主要成分为A12 O3、SiO2和Fe2O3)为原料制备水质净化剂PAC{[A12(OH)nC16-n]m(n<6,m为聚合度)}的过程如图.下列说法正确的是( )| A. | 试剂X为H2SO4 | B. | 滤渣主要成分为Fe(OH)3、H2 SiO3 | ||
| C. | 调pH过高或过低均会减少PAC生成 | D. | 滤液浓缩聚合过程发生了加聚反应 |
13.目前人工合成高效青蒿素主要采用青蒿酸为原料半合成法.青蒿酸的结构简式如图A所示.下列有关说法正确的是( )
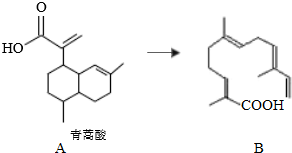

| A. | 青蒿酸的分子式为C15H20O2 | |
| B. | 1mol青蒿酸最多可与3molH2加成 | |
| C. | 青蒿酸与B互为同分异构体 | |
| D. | 苯环上连有-CHO和-OH、分子中有6种不同化学环境氢的青蒿酸的同分异构体只有2种 |
20.有机物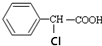 有多种同分异构体,其中属于酯类且氯原子直接连在苯环上的同分异构体有多少种(不考虑立体异构)( )
有多种同分异构体,其中属于酯类且氯原子直接连在苯环上的同分异构体有多少种(不考虑立体异构)( )
 有多种同分异构体,其中属于酯类且氯原子直接连在苯环上的同分异构体有多少种(不考虑立体异构)( )
有多种同分异构体,其中属于酯类且氯原子直接连在苯环上的同分异构体有多少种(不考虑立体异构)( )| A. | 6种 | B. | 9种 | C. | 15种 | D. | 19种 |
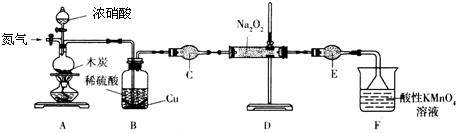
10.将浓盐酸滴入KMnO4溶液,产生黄绿色气体,溶液的紫红色褪去,向反应后的溶液中加入NaBiO3,溶液又变为紫红色,BiO3-反应后变为无色的Bi3+.据此判断下列说法正确的是( )
| A. | 滴加盐酸时,HCl是还原剂,Cl2是还原产物 | |
| B. | 已知Bi为第ⅤA族元素,上述实验说明Bi具有较强的非金属性 | |
| C. | 若有0.1 mol NaBiO3参加了反应,则整个过程转移电子0.8 NA | |
| D. | 此实验条件下,物质的氧化性:NaBiO3>KMnO4>Cl2 |
11.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1 mol-OH中含有10 NA个电子 | |
| B. | 1 L 1 mol•L-1CH3COONa溶液中含有NA个CH3COO- | |
| C. | 28g晶体硅中含有共价键数目为2NA个 | |
| D. | 常温常压下11.2 L甲烷气体含有的分子数为0.5NA |
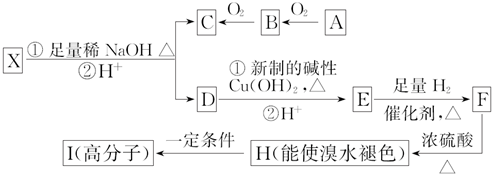
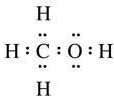 ;I的结构简式为
;I的结构简式为 .
.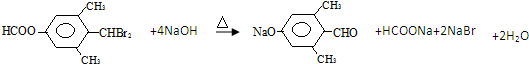 ;
; 任意一种.
任意一种.