题目内容
15.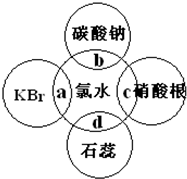 氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量).
氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量).①能证明氯水具有漂白性的是d(填“a、b、c或d”).
②C过程中的现象是有白色沉淀生成.
③a过程中的化学方程式为Cl2+2KBr=2Cl-+Br2.
分析 氯水含多种微粒,其中有H2O、Cl2、HClO、Cl-、H+、OH-(极少量,水微弱电离出来的).
氯水的性质取决于其组成的微粒:
1)强氧化性:Cl2是新制氯水的主要成分,实验室常用氯水代替氯气,如氯水中的氯气能与KI,KBr、FeCl2、SO2、Na2SO3等物质反应.
2)漂白、消毒性:氯水中的Cl2和HClO均有强氧化性,一般在应用其漂白和消毒时,应考虑HClO,HClO的强氧化性将有色物质氧化成无色物质,不可逆.
3)酸性:氯水中含有HCl和HClO,故可被NaOH中和,盐酸还可与NaHCO3,CaCO3等反应.
4)不稳定性:HClO不稳定光照易分解. 因此久置氯水(浅黄绿色)会变成稀盐酸(无色)失去漂白性.
5)沉淀反应:加入AgNO3溶液有白色沉淀生成(氯水中有Cl-),据此解答.
解答 解:①氯水中的HClO有强氧化性,一般在应用其漂白时,HClO的强氧化性将有色物质氧化成无色物质,本题中氯水能使石蕊试液先变红,后褪色,
故答案为:d;
②氯水中有Cl-,加入AgNO3溶液有白色沉淀生成,生成AgCl沉淀,
故答案为:有白色沉淀生成;
③氯气具有强的氧化性,能够氧化溴化钾生成氯化钾和溴单质,离子方程式:Cl2+2KBr=2Cl-+Br2;
故答案为:Cl2+2KBr=2Cl-+Br2;
点评 本题考查氯水的性质,明确氯水所含微粒及性质是解题关键,题目难度不大,注重基础知识的积累.

练习册系列答案
相关题目
12.已知某烃A相对氢气的密度为42,且该烃不能使溴的CCl4溶液褪色.则A的可能结构共有(不考虑立体异构)( )
| A. | 9种 | B. | 10种 | C. | 11种 | D. | 12种 |
13.目前人工合成高效青蒿素主要采用青蒿酸为原料半合成法.青蒿酸的结构简式如图A所示.下列有关说法正确的是( )
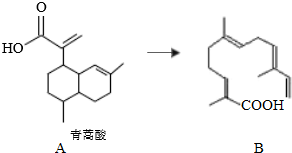

| A. | 青蒿酸的分子式为C15H20O2 | |
| B. | 1mol青蒿酸最多可与3molH2加成 | |
| C. | 青蒿酸与B互为同分异构体 | |
| D. | 苯环上连有-CHO和-OH、分子中有6种不同化学环境氢的青蒿酸的同分异构体只有2种 |
3. 某研究性学习小组用PH=1的盐酸滴定25.00mL未知物质的量浓度的NaOH溶液,从而求出该NaOH溶液的PH值(选用酚酞作为指示剂)
某研究性学习小组用PH=1的盐酸滴定25.00mL未知物质的量浓度的NaOH溶液,从而求出该NaOH溶液的PH值(选用酚酞作为指示剂)
①实验过程中需要使用的仪器有铁架台、滴定管夹、碱式滴定管、胶头滴管、酸式滴定管、锥形瓶,
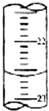
②如图,是某次滴定时的滴定管中的液面,其读数为22.60mL.
③如何判断滴定到达终点当滴加最后一滴盐酸,溶液的颜色由黄色变为橙色,且在半分钟内不变色.
③根据下列数据:
请计算待测NaOH溶液的浓度(保留两位小数)0.0800mol/L.
④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有:BD.
A、滴定终点读数时俯视读数
B、酸式滴定管使用前,水洗后未用盐酸溶液润洗
C、锥形瓶水洗后未干燥
D、酸式滴定管尖嘴部分有气泡,滴定后消失.
 某研究性学习小组用PH=1的盐酸滴定25.00mL未知物质的量浓度的NaOH溶液,从而求出该NaOH溶液的PH值(选用酚酞作为指示剂)
某研究性学习小组用PH=1的盐酸滴定25.00mL未知物质的量浓度的NaOH溶液,从而求出该NaOH溶液的PH值(选用酚酞作为指示剂)①实验过程中需要使用的仪器有铁架台、滴定管夹、碱式滴定管、胶头滴管、酸式滴定管、锥形瓶,
②如图,是某次滴定时的滴定管中的液面,其读数为22.60mL.
③如何判断滴定到达终点当滴加最后一滴盐酸,溶液的颜色由黄色变为橙色,且在半分钟内不变色.
③根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 4.00 | 24.10 |
④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有:BD.
A、滴定终点读数时俯视读数
B、酸式滴定管使用前,水洗后未用盐酸溶液润洗
C、锥形瓶水洗后未干燥
D、酸式滴定管尖嘴部分有气泡,滴定后消失.
10.将浓盐酸滴入KMnO4溶液,产生黄绿色气体,溶液的紫红色褪去,向反应后的溶液中加入NaBiO3,溶液又变为紫红色,BiO3-反应后变为无色的Bi3+.据此判断下列说法正确的是( )
| A. | 滴加盐酸时,HCl是还原剂,Cl2是还原产物 | |
| B. | 已知Bi为第ⅤA族元素,上述实验说明Bi具有较强的非金属性 | |
| C. | 若有0.1 mol NaBiO3参加了反应,则整个过程转移电子0.8 NA | |
| D. | 此实验条件下,物质的氧化性:NaBiO3>KMnO4>Cl2 |
20.下列物质中属于纯净物的是( )
| A. | 天然气 | B. | 铝热剂 | C. | 氨气 | D. | 氯水 |
7.下列卤代烃能发生消去反应且消去产物唯一的是( )
| A. | CH3CH2CH2Br | B. | (CH3)3CCH2Br | C. | 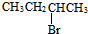 | D. | 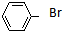 |
4.下列有关实验的叙述正确的是( )
| A. | 检验溶液中SO42-的方法是:先加入BaCl2溶液,再加盐酸 | |
| B. | 从溴水中提纯单质溴的方法是:先用CCl4萃取,分液后再蒸馏 | |
| C. | 硫化钠溶液中通入硫化氢气体不发生化学反应 | |
| D. | 除去CO2中少量HCl的方法是:将混合气体通过盛有饱和NaHSO3溶液的洗气瓶 |
5.下列有关电解质的说法不正确的是( )
| A. | K+、Mg2+、I-、NO3-在无色溶液中能大量共存 | |
| B. | K+、Na+、CO32-、NO3-在酸性溶液中不能大量共存 | |
| C. | CO2与少量烧碱溶液反应:CO2+2OH-=CO32-+H2O | |
| D. | 向AlCl3溶液中加入过量的氨水溶液Al3++3NH3.H2O=Al(OH)3↓+3NH4+ |