题目内容
13.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生.下列属于未来新能源标准的是( )①天然气 ②核能 ③石油 ④太阳能 ⑤风能 ⑥氢能.
| A. | ①②③ | B. | ④⑤⑥ | C. | ①③⑤ | D. | ②④⑥ |
分析 煤、石油、天然气是化石燃料,太阳能、核能、地热能、潮汐能、风能、氢能、生物质能等都是新能源.
解答 解:煤、石油、天然气是化石能源,对环境的污染较重,不能再生,不是新能源,常见新能源有:太阳能、核能、地热能、潮汐能、风能、氢能、生物质能等,资源丰富,在使用时对环境无污染或污染很小,且可以再生.
故选B.
点评 本题考查新能源,题目难度不大,注意加强基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.下列叙述正确的是( )
| A. | 在中和热的测定实验中,应将碱液缓慢倒入酸液中,使反应充分进行 | |
| B. | 用NaOH标准溶液滴定醋酸溶液至中性时,醋酸则被完全中和 | |
| C. | 将Na2S2O3溶液和稀硫酸混合,可通过观察产生气泡的快慢来判断化学反应速率 | |
| D. | 将铁钉放试管中,加入2mL水、3滴稀醋酸和1滴K3[Fe(CN)6]溶液,不久铁钉周围出现蓝色沉淀 |
4.查阅资料:无水醋酸钠是无色无味的结晶体,在空气中可被风化,可燃.用无水醋酸钠与碱石灰加热可以制得X气体.并作相应的实验:
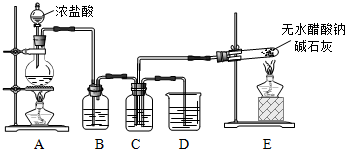
(1)装置E中反应方程式是CH3COONa+NaOH$→_{△}^{CaO}$Na2CO3+X↑,X的化学式是CH4.
(2)在C中收集气体X和Cl2为1:1体积混合,然后在光照下反应:
①B装置的作用是除去Cl2中含有的HCl;
②C装置所盛放试剂是饱和食盐水;光照后所得产物有CH3Cl、CH2Cl2、CHCl3、CCl4、HCl;
(3)设计一个实验方案,验证产物中生成了一种无机物:光照后,取C和D中液体各少许,分别加入两支试管中,再分别滴加2滴石蕊溶液,C中溶液红色更深;或用pH试纸测定C和D中溶液的pH等
(4)某学生为了测定X的组成进行实验探究,选用了下列仪器:
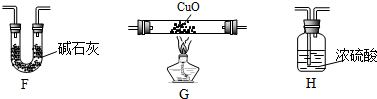
①该同学依次连接的合理顺序是E、G、H、F;
②该同学测定的相关数据是:
数据是否完全,说明原因数据是不完全,因为只能确定有机物中的碳氢元素含量,不能确定是否含有氧元素,应称取C装置实验前后的质量;
该测定含氢量是否有偏差?若有偏差,请说明原因F中吸收的是CO2,CO2质量33.6g-22.5g=11.1g,n(C)=$\frac{11.1g}{44g/mol}$=0.252mol;H中吸收的是水蒸气,H2O质量51.4g-42.4g=9.0g,n(H)=$\frac{9.0g}{18g/mol}$×2=1.0mol;
故n(C):n(H)>1:4.原因是F装置后面与空气接触,空气中的水蒸气和CO2进入了B装置,造成含碳量偏大.

(1)装置E中反应方程式是CH3COONa+NaOH$→_{△}^{CaO}$Na2CO3+X↑,X的化学式是CH4.
(2)在C中收集气体X和Cl2为1:1体积混合,然后在光照下反应:
①B装置的作用是除去Cl2中含有的HCl;
②C装置所盛放试剂是饱和食盐水;光照后所得产物有CH3Cl、CH2Cl2、CHCl3、CCl4、HCl;
(3)设计一个实验方案,验证产物中生成了一种无机物:光照后,取C和D中液体各少许,分别加入两支试管中,再分别滴加2滴石蕊溶液,C中溶液红色更深;或用pH试纸测定C和D中溶液的pH等
(4)某学生为了测定X的组成进行实验探究,选用了下列仪器:

①该同学依次连接的合理顺序是E、G、H、F;
②该同学测定的相关数据是:
| 装置 | 实验前的质量/g | 实验后的质量/g |
| F | 22.5 | 33.6 |
| H | 42.4 | 51.4 |
该测定含氢量是否有偏差?若有偏差,请说明原因F中吸收的是CO2,CO2质量33.6g-22.5g=11.1g,n(C)=$\frac{11.1g}{44g/mol}$=0.252mol;H中吸收的是水蒸气,H2O质量51.4g-42.4g=9.0g,n(H)=$\frac{9.0g}{18g/mol}$×2=1.0mol;
故n(C):n(H)>1:4.原因是F装置后面与空气接触,空气中的水蒸气和CO2进入了B装置,造成含碳量偏大.
1.某元素原子的结构示意图为 ,关于该原子说法正确的是( )
,关于该原子说法正确的是( )
 ,关于该原子说法正确的是( )
,关于该原子说法正确的是( )| A. | 核电荷数为32 | B. | 核外电子数为6 | ||
| C. | 有3个电子层 | D. | 比其阴离子多2个电子 |
8.100℃时,KW=1.0×10-12,若在100℃时某溶液中的c(H+)=1.0×10-7 mol•L-1,则该溶液( )
| A. | 呈中性 | B. | 呈碱性 | C. | 呈酸性 | D. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=1 |
18.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在某密闭容器中加入0.5 molN2和1.5 mol H2,充分反应后有的N-H键数为3NA | |
| B. | 标准状况下,2.24 L SO3含有的原子数为0.4 NA | |
| C. | 71 g氯气与足量铁反应过程中转移的电子数为2NA | |
| D. | NA个Fe3+完全水解可以得到NA个氢氧化铁胶体粒子 |
5.下列说法正确的是( )
| A. | 红磷转化为白磷,属于物理变化 | |
| B. | 石墨导电、金刚石不导电,故二者不是同素异形体 | |
| C. | O2和O3分子式不同,结构相同 | |
| D. | 单质硫有S2、S4、S6等,它们都是硫的同素异形体 |
2.分子式为C8H10的芳香烃,苯环上的一氯代物只有一种,该芳香烃的名称是( )
| A. | 乙苯 | B. | 对二甲苯 | C. | 间二甲苯 | D. | 邻二甲苯 |
3. Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍.下列说法正确的是( )
Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍.下列说法正确的是( )
 Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍.下列说法正确的是( )
Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍.下列说法正确的是( )| A. | 原子半径大小顺序为r(Q)>r(R)>r(T)>r(M)>r(W) | |
| B. | Q、W的单核离子的核外电子数相等 | |
| C. | 五种元素均能形成氢化物 | |
| D. | W的氢化物水溶液酸性最强,说明W的非金属性在五种元素中最强 |