题目内容
18.NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 在某密闭容器中加入0.5 molN2和1.5 mol H2,充分反应后有的N-H键数为3NA | |
| B. | 标准状况下,2.24 L SO3含有的原子数为0.4 NA | |
| C. | 71 g氯气与足量铁反应过程中转移的电子数为2NA | |
| D. | NA个Fe3+完全水解可以得到NA个氢氧化铁胶体粒子 |
分析 A.合成氨反应为可逆反应,可逆反应不能进行到底;
B.标况下三氧化硫不是气体;
C.氯气与铁反应生成氯化铁,氯气不足,依据氯气的量计算转移电子数;
D.一个氢氧化铁胶粒是多个氢氧化铁的聚集体.
解答 解:A.在某密闭容器中加入0.5 molN2和1.5 mol H2,生成氨气小于1mol,充分反应后有的N-H键数小于3NA,故A错误;
B.标况下三氧化硫不是气体,不能使用气体摩尔体积,故B错误;
C.71g氯气即1mol,与足量铁反应转移的电子数为2NA,故C正确;
D.一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故得到的氢氧化铁胶粒个数小于NA个,故D错误;
故选:C.
点评 本题考查阿伏加德罗常数,明确以物质的量为核心的计算公式是解题关键,解题时注意物质的状态、存在的条件、物质的性质和分子的组成等因素,题目难度不大.

练习册系列答案
相关题目
9.下列说法正确的是( )
| A. | 有的共价化合物在液态时也能导电 | |
| B. | 含有离子键的化合物中,也可能还含有共价键 | |
| C. | 形成离子键的微粒必须是金属阳离子与阴离子 | |
| D. | 非金属元素形成的化合物一定不存在离子键 |
6.在氨水中存在NH3•H2O?NH4++OH-的平衡,若要使平衡向逆方向移动,同时使c(OH-)增大,应加入( )
| A. | 氯化铵固体 | B. | 硫酸 | C. | NaOH固体 | D. | 大量水 |
13.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生.下列属于未来新能源标准的是( )
①天然气 ②核能 ③石油 ④太阳能 ⑤风能 ⑥氢能.
①天然气 ②核能 ③石油 ④太阳能 ⑤风能 ⑥氢能.
| A. | ①②③ | B. | ④⑤⑥ | C. | ①③⑤ | D. | ②④⑥ |
10.下列关于物质性质的比较中不正确的是( )
| A. | 碱性:KOH>NaOH>LiOH | B. | 金属性:Na>Mg>Al | ||
| C. | 原子半径:Na>S>O | D. | 酸性强弱:H3PO4>H2SO4>HClO4 |
7.下列说法正确的是( )
| A. | 某有机物燃烧只生成CO2和H2O,且二者物质的量相等,则此有机物的组成为CnH2n | |
| B. | 一种烃在足量的氧气中燃烧并通过碱石灰,减少的体积就是生成水蒸气的体积 | |
| C. | 某气态烃CxHy与足量O2恰好完全反应,如果反应前后气体体积不变(温度>100℃),则y=4,若体积减少,则y>4,否则y<4 | |
| D. | 相同质量的烃,完全燃烧,消耗的O2越多,则烃中氢元素的百分含量越高 |
8.科学家通过探寻矿物X推测外星球上是否曾经存在水.某兴趣小组为分析矿物X中的常见离子,将其溶于稀硝酸,并将所得溶液进行实验,下列依据实验现象得出的结论正确的是( )
| A. | 用铂丝蘸取少量溶液进行焰色反应,火焰呈紫色,说明矿物X中含K+ | |
| B. | 取少量溶液向其中滴加NaOH溶液,加热,用湿润红色石蕊试纸检验生成的气体,试纸变蓝,说明矿物X中含NH4+ | |
| C. | 取少量溶液向其中滴加KSCN溶液,溶液变为血红色,说明矿物X中含Fe3+ | |
| D. | 取少量溶液向其中滴加盐酸酸化的BaCl2溶液,有白色沉淀产生,说明矿物X中含SO42- |
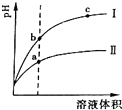 常温下有0.1mol•L-1五种溶液NaOH、NH3•H2O、CH3COOH、HCl、NH4HSO4.
常温下有0.1mol•L-1五种溶液NaOH、NH3•H2O、CH3COOH、HCl、NH4HSO4.