题目内容
某一化学反应在不同条件下的能量变化曲线如图所示.下列说法正确的是( )
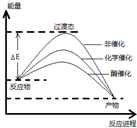

| A、化学催化比酶催化的效果好 |
| B、使用不同催化剂可以改变反应的能耗 |
| C、反应物的总能量低于生成物的总能量 |
| D、使用不同催化剂可以改变反应的热效应 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A.根据催化剂是通过降低反应的活化能来加快化学反应速率的,活化能越低,催化的效果越好;
B.根据不同催化剂的活化能不同;
C.由图可知:反应物的总能量高于生成物的总能量;
D.根据焓变=生成物的总能量-反应物的总能量.
B.根据不同催化剂的活化能不同;
C.由图可知:反应物的总能量高于生成物的总能量;
D.根据焓变=生成物的总能量-反应物的总能量.
解答:
解:A.酶催化的活化能小于比化学催化的活化能,所以酶催化比化学催化的效果好,故A错误;
B.使用不同催化剂,反应所需要的能量不同,即可以改变反应的能耗,故B正确;
C.由图可知:反应物的总能量高于生成物的总能量,故C错误;
D.使用不同催化剂,反应物的总能量和生成物的总能量都没有变化,而焓变=生成物的总能量-反应物的总能量,所以使用不同催化剂不会改变该反应的焓变,故D错误;
故选C.
B.使用不同催化剂,反应所需要的能量不同,即可以改变反应的能耗,故B正确;
C.由图可知:反应物的总能量高于生成物的总能量,故C错误;
D.使用不同催化剂,反应物的总能量和生成物的总能量都没有变化,而焓变=生成物的总能量-反应物的总能量,所以使用不同催化剂不会改变该反应的焓变,故D错误;
故选C.
点评:本题考查了化学反应中催化剂的作用,掌握催化剂在反应中的原理是解题的根本.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
下列变化中,需要加入适当的氧化剂才能完成的是( )
| A、SO3→H2SO4 |
| B、CuO→Cu |
| C、Fe→FeCl3 |
| D、Cl2→ClO- |
已知工业合成氨:2N2(g)+6H2(g)?4NH3(g)△H=-184.8kJ/mol.一定条件下,现有容积相同且恒容的密闭容器甲与乙:①向甲中通入1mol N2和3mol H2,达到平衡时放出热量Q1 kJ;②向乙中通入0.5mol N2和1.5mol H2,达到平衡时放出热量Q2kJ.则下列关系式正确的是( )
| A、92.4=Q1<2Q2 |
| B、92.4>Ql>2Q2 |
| C、Q1=2Q2=92.4 |
| D、Q1=2Q2<92.4 |
某反应的离子方程式为Ca2++CO32-═CaCO3↓,对该反应的下列说法不正确的是( )
| A、该反应可能是化合反应,也可能是氧化还原反应 |
| B、该反应一定是复分解反应,且属于非氧化还原反应 |
| C、该反应可能是CaCl2+Na2CO3═CaCO3↓+2NaCl |
| D、该反应可能是Ca(OH)2+K2CO3═CaCO3↓+2KOH |
X、Y、Z是3种短周期元素,其中X、Y位于同一族,Y、Z处于同一周期.X原子的外围电子排布式为nSnnPn+2.Z原子的核电荷数是最外层电子数的三倍.下列说法正确的是( )
| A、原子序数由大到小的顺序为Z<Y<X |
| B、Y元素最高价氧化物对应水化物的化学式可表示为H3YO4 |
| C、3种元素的气态氢化物中Z的气态氢化物最稳定 |
| D、原子半径由大到小的顺序为Z>Y>X |
 E~N等元素在周期表中的相对位置如下表.E与K的原子序数相差4,K的一种单质是空气中含量最多的物质,H与N属同周期元素,下列判断不正确的是( )
E~N等元素在周期表中的相对位置如下表.E与K的原子序数相差4,K的一种单质是空气中含量最多的物质,H与N属同周期元素,下列判断不正确的是( )| A、K的氢化物水溶液显碱性 |
| B、F的单质与氧气反应只生成一种氧化物 |
| C、H与N的原子核外电子数相差14 |
| D、最高价氧化物的水化物酸性:K>L>M |
稀溶液一般有依数性,即在一定温度下,相同体积的溶液中溶质粒子数目越多,蒸气压下降数值越大.浓度均为0.1mol?L-1的下列稀溶液,其蒸气压最小的是( )
| A、H2SO3溶液 |
| B、C6H12O6溶液 |
| C、NaCl溶液 |
| D、NH3?H2O溶液 |