题目内容
稀溶液一般有依数性,即在一定温度下,相同体积的溶液中溶质粒子数目越多,蒸气压下降数值越大.浓度均为0.1mol?L-1的下列稀溶液,其蒸气压最小的是( )
| A、H2SO3溶液 |
| B、C6H12O6溶液 |
| C、NaCl溶液 |
| D、NH3?H2O溶液 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:亚硫酸和一水合氨是弱电解质,不完全电离,葡萄糖是非电解质,不电离,NaCl是强电解质完全电离,据此分析溶液中离子浓度.
解答:
解:在一定温度下,相同体积的溶液中溶质粒子数目越多,蒸气压下降数值越大,亚硫酸和一水合氨是弱电解质,电离程度很小,0.1mol?L-1的溶液中其阴离子和阳离子的浓度远远小于0.1mol/L,葡萄糖是非电解质,不电离,NaCl是强电解质,完全电离,0.1mol?L-1的NaCl溶液中,阴两点和阳离子浓度均为0.1mol/L,所以上述稀溶液中,NaCl溶液中溶质粒子数目最多,其蒸气压最小,
故选C.
故选C.
点评:本题属于信息给予题,据题给信息,结合电解质和非电解质、强电解质和弱电解质进行分析.

练习册系列答案
相关题目
某一化学反应在不同条件下的能量变化曲线如图所示.下列说法正确的是( )
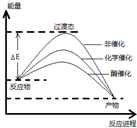

| A、化学催化比酶催化的效果好 |
| B、使用不同催化剂可以改变反应的能耗 |
| C、反应物的总能量低于生成物的总能量 |
| D、使用不同催化剂可以改变反应的热效应 |
下列各项叙述,正确的是( )
A、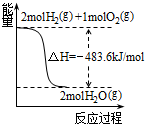 可得H2的燃烧热为483.6kJ?mol-1 |
B、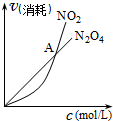 表示恒温恒容条件下发生的可逆反应2NO2(g)═N2O4(g),各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 |
C、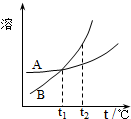 表示A、B两物质的溶解度随温度的变化情况,将t1℃时的A、B饱和溶液分别升温至t2℃时,溶质的质量分数B>A |
D、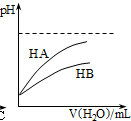 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加入水量的变化,则常温时同浓度的NaA溶液的pH小于NaB溶液 |
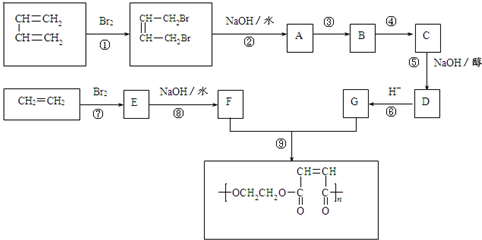
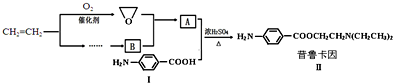
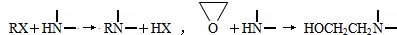
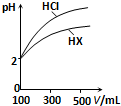 水是极弱的电解质,改变温度或加入某些电解质会影响水的电离.请回答下列问题:
水是极弱的电解质,改变温度或加入某些电解质会影响水的电离.请回答下列问题: