题目内容
已知工业合成氨:2N2(g)+6H2(g)?4NH3(g)△H=-184.8kJ/mol.一定条件下,现有容积相同且恒容的密闭容器甲与乙:①向甲中通入1mol N2和3mol H2,达到平衡时放出热量Q1 kJ;②向乙中通入0.5mol N2和1.5mol H2,达到平衡时放出热量Q2kJ.则下列关系式正确的是( )
| A、92.4=Q1<2Q2 |
| B、92.4>Ql>2Q2 |
| C、Q1=2Q2=92.4 |
| D、Q1=2Q2<92.4 |
考点:反应热的大小比较
专题:化学反应中的能量变化
分析:反应为可逆反应,向密闭容器甲中通入1molN2和3molH2,达平衡时放出热量 Q1<Q,甲与乙相比较,甲相当于在乙的基础上增大压强,平衡向正反应方向移动,则甲转化率大于乙,以此解答该题.
解答:
解:反应为可逆反应,向密闭容器甲中通入1molN2和3molH2,达平衡时放出热量 Q1<92.4,甲与乙相比较,甲相当于在乙的基础上增大压强,平衡向正反应方向移动,则甲转化率大于乙,如转化率相等,则Q1=2Q2,而转化率越大,则反应的热量越多,则Q1>2Q2,所以2Q2<Q1<92.4;
故选:B.
故选:B.
点评:本题综合考查化学平衡移动问题,为高考常见题型,侧重于考查学生的分析能力,本题可从压强对平衡移动影响的角度分析,难度中等.

练习册系列答案
相关题目
生活中处处有化学,下列有关说法正确的是( )
| A、糖类、蛋白质、脂肪都是人类需要的营养物质 |
| B、饮用矿泉水瓶、一次性水杯的主要成分是聚氯乙烯 |
| C、冬天用纯甘油涂抹在手和面部可以防止皮肤干燥和开裂 |
| D、大米富含淀粉,大米煮成粥后淀粉变成了葡萄糖 |
关于0.1mol?L-1 NaHCO3溶液,下列说法正确的是( )
| A、溶质水解反应:HCO3-+H2?H3O++CO32- |
| B、离子浓度关系:c(Na+)+c(H+)═c(OH-)+c(HCO3-)+c(CO32-) |
| C、微粒浓度关系:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-) |
| D、微粒浓度关系:c(Na+)═2[c(H2CO3)+c(HCO3-)+c(CO32-)] |
下列物质之间反应,不可能发生爆炸的是( )
| A、H2与F2 |
| B、H2与I2 |
| C、H2与O2 |
| D、Na与S |
如图图示与对应的叙述相符的是( )


| A、由图甲可以判断:对于反应aA(g)+bB(g)?cC(g),若T1>T2,则a+b=c且△H<0 |
| B、图乙表示压强对可逆反应2A(g)+2 B(g)?3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| C、根据图丙,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量NaOH溶液,调节pH≈4 |
| D、图丁表示用0.1000mol/LNaOH溶液滴定20.00mL0.1000mol/L醋酸溶液得到的滴定曲线 |
下列说法正确的是( )
| A、弱碱溶于水后能促进水的电离 |
| B、盐溶于水后一定能促进水的电离 |
| C、任何条件下,只要pH>7,溶液就一定显碱性 |
| D、任何条件下,只要c(H+)>c(OH-),溶液就一定显酸性 |
如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面图.下列说法正确的是( )
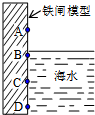

| A、该电化腐蚀为析氢腐蚀 |
| B、图中生成铁锈最多的是C区域 |
| C、A区域比B区域更易腐蚀 |
| D、铁闸中的负极的电极反应:Fe-2e-=Fe2+ |
某一化学反应在不同条件下的能量变化曲线如图所示.下列说法正确的是( )
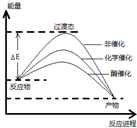

| A、化学催化比酶催化的效果好 |
| B、使用不同催化剂可以改变反应的能耗 |
| C、反应物的总能量低于生成物的总能量 |
| D、使用不同催化剂可以改变反应的热效应 |