题目内容
根据反应3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,回答下列问题:
(1)还原剂是 ,还原产物是 ,氧化剂是 ,氧化产物是 .
(2)氧化剂与氧化产物的物质的量比是 .
(3)当有2mol HNO3被还原时,被氧化的物质的质量为 ,反应中转移的电子数为 .
(1)还原剂是
(2)氧化剂与氧化产物的物质的量比是
(3)当有2mol HNO3被还原时,被氧化的物质的质量为
考点:氧化还原反应
专题:
分析:8HNO3+3Cu═3Cu(NO3)2+2NO↑+4H2O反应中,Cu元素的化合价由0升高为+2价,N元素的化合价由+5价降低为+2价,以此来解答
解答:
解:(1)8HNO3+3Cu═3Cu(NO3)2+2NO↑+4H2O反应中,Cu元素的化合价升高,则Cu为还原剂,被氧化,对应的Cu(NO3)2为氧化产物;N元素的化合价降低,则HNO3为氧化剂,被还原,则NO为还原产物,
故答案为:Cu;NO;HNO3;3Cu(NO3)2;
(2)反应中8mol硝酸中有2mol作氧化剂,生成氧化产物Cu(NO3)2为3mol,则氧化剂与氧化产物的物质的量比是2:3;
故答案为:2:3;
(3)由方程式可知当有2mol HNO3被还原时,3molCu被氧化,则被氧化的Cu的质量为3mol×64g/mol=192g,转移的电子为6mol,即6NA.
故答案为:192g;6NA.
故答案为:Cu;NO;HNO3;3Cu(NO3)2;
(2)反应中8mol硝酸中有2mol作氧化剂,生成氧化产物Cu(NO3)2为3mol,则氧化剂与氧化产物的物质的量比是2:3;
故答案为:2:3;
(3)由方程式可知当有2mol HNO3被还原时,3molCu被氧化,则被氧化的Cu的质量为3mol×64g/mol=192g,转移的电子为6mol,即6NA.
故答案为:192g;6NA.
点评:本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,注意从元素化合价角度分析,题目难度不大.

练习册系列答案
相关题目
氧化还原反应与四种基本反应类型的关系如图所示.下列化学反应属于阴影部分的是( )
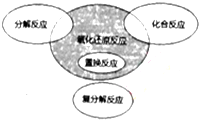

A、SiO2+2C
| ||||
| B、4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||||
C、2NaHCO3
| ||||
D、CuO+CO
|
如图图示与对应的叙述相符的是( )


| A、由图甲可以判断:对于反应aA(g)+bB(g)?cC(g),若T1>T2,则a+b=c且△H<0 |
| B、图乙表示压强对可逆反应2A(g)+2 B(g)?3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| C、根据图丙,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量NaOH溶液,调节pH≈4 |
| D、图丁表示用0.1000mol/LNaOH溶液滴定20.00mL0.1000mol/L醋酸溶液得到的滴定曲线 |
如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面图.下列说法正确的是( )
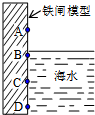

| A、该电化腐蚀为析氢腐蚀 |
| B、图中生成铁锈最多的是C区域 |
| C、A区域比B区域更易腐蚀 |
| D、铁闸中的负极的电极反应:Fe-2e-=Fe2+ |
下列不涉及氧化还原反应的是( )
| A、自然界中“氮的固定” |
| B、用铂丝蘸取NaCl溶液进行焰色反应 |
| C、食物腐败变质 |
| D、铜铸塑像上出现铜绿[Cu2(OH)2CO3] |
某一化学反应在不同条件下的能量变化曲线如图所示.下列说法正确的是( )
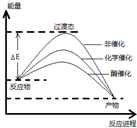

| A、化学催化比酶催化的效果好 |
| B、使用不同催化剂可以改变反应的能耗 |
| C、反应物的总能量低于生成物的总能量 |
| D、使用不同催化剂可以改变反应的热效应 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3 NA | ||
| B、1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | ||
| C、常温下,56 g铁片投入足量浓H2SO4中生成NA个SO2分子 | ||
D、将CO2通过Na2O2使其增重a g,反应中转移的电子数为
|