题目内容
下列变化中,需要加入适当的氧化剂才能完成的是( )
| A、SO3→H2SO4 |
| B、CuO→Cu |
| C、Fe→FeCl3 |
| D、Cl2→ClO- |
考点:氧化还原反应,重要的氧化剂
专题:氧化还原反应专题
分析:需要加入适当的氧化剂才能实现,说明给予物质作还原剂,在反应中失电子化合价升高,据此分析解答.
解答:
解:需要加入适当的氧化剂才能实现,说明给予物质作还原剂,在反应中失电子化合价升高,
A.该反应中S元素化合价都是+6价,所以不发生氧化还原反应,故A错误;
B.该反应中Cu元素化合价由+2价变为0价,所以CuO得电子化合价降低而作氧化剂,故B错误;
C.该反应中Fe元素化合价由0价变为+3价,所以Fe失电子化合价升高而作还原剂,故C正确;
D.该反应中Cl元素化合价由0价变为+1价,所以氯气失电子作还原剂,但不需要加入氧化剂也能实现,故D错误;
故选C.
A.该反应中S元素化合价都是+6价,所以不发生氧化还原反应,故A错误;
B.该反应中Cu元素化合价由+2价变为0价,所以CuO得电子化合价降低而作氧化剂,故B错误;
C.该反应中Fe元素化合价由0价变为+3价,所以Fe失电子化合价升高而作还原剂,故C正确;
D.该反应中Cl元素化合价由0价变为+1价,所以氯气失电子作还原剂,但不需要加入氧化剂也能实现,故D错误;
故选C.
点评:本题以氧化还原反应为载体考查氧化剂、还原剂,侧重考查基本概念,根据元素化合价变化分析解答即可,知道常见元素化合价,题目难度不大.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
下列实验装置或操作正确的是( )
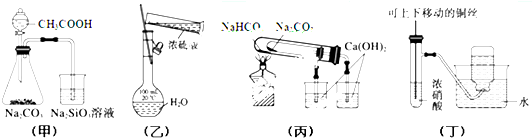

| A、用甲图装置验证CH3COOH、H2CO3和H2SiO3的酸性强弱 |
| B、用乙图装置配制一定浓度的稀硫酸 |
| C、用丙图装置验证NaHCO3和Na2CO3的热稳定性 |
| D、用丁图装置制备并收集少量NO2气体 |
生活中处处有化学,下列有关说法正确的是( )
| A、糖类、蛋白质、脂肪都是人类需要的营养物质 |
| B、饮用矿泉水瓶、一次性水杯的主要成分是聚氯乙烯 |
| C、冬天用纯甘油涂抹在手和面部可以防止皮肤干燥和开裂 |
| D、大米富含淀粉,大米煮成粥后淀粉变成了葡萄糖 |
有关化学资源的合成、利用与开发的叙述合理的是( )
| A、大量使用化肥和农药,能不断提高农作物产量 |
| B、通过有机合成,可以制造出比钢铁更强韧的新型材料 |
| C、安装煤炭燃烧过程的“固硫”装置,主要是为了提高煤的利用率 |
| D、开发利用可燃冰(固态甲烷水合物),有助于海洋生态环境的治理 |
氧化还原反应与四种基本反应类型的关系如图所示.下列化学反应属于阴影部分的是( )
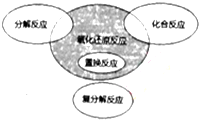

A、SiO2+2C
| ||||
| B、4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||||
C、2NaHCO3
| ||||
D、CuO+CO
|
分子式为C7H8O的芳香化合物中,与FeCl3溶液混合显紫色和不显紫色的物质分别有( )
| A、2种和1种 |
| B、2种和3种 |
| C、3种和2种 |
| D、3种和1种 |
关于0.1mol?L-1 NaHCO3溶液,下列说法正确的是( )
| A、溶质水解反应:HCO3-+H2?H3O++CO32- |
| B、离子浓度关系:c(Na+)+c(H+)═c(OH-)+c(HCO3-)+c(CO32-) |
| C、微粒浓度关系:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-) |
| D、微粒浓度关系:c(Na+)═2[c(H2CO3)+c(HCO3-)+c(CO32-)] |
下列物质之间反应,不可能发生爆炸的是( )
| A、H2与F2 |
| B、H2与I2 |
| C、H2与O2 |
| D、Na与S |
某一化学反应在不同条件下的能量变化曲线如图所示.下列说法正确的是( )
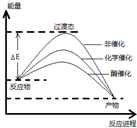

| A、化学催化比酶催化的效果好 |
| B、使用不同催化剂可以改变反应的能耗 |
| C、反应物的总能量低于生成物的总能量 |
| D、使用不同催化剂可以改变反应的热效应 |