题目内容
某反应的离子方程式为Ca2++CO32-═CaCO3↓,对该反应的下列说法不正确的是( )
| A、该反应可能是化合反应,也可能是氧化还原反应 |
| B、该反应一定是复分解反应,且属于非氧化还原反应 |
| C、该反应可能是CaCl2+Na2CO3═CaCO3↓+2NaCl |
| D、该反应可能是Ca(OH)2+K2CO3═CaCO3↓+2KOH |
考点:氧化还原反应,化学方程式的书写
专题:
分析:A.反应中没有元素化合价的变化;
B.属于复分解反应;
C.写出CaCl2+Na2CO3═CaCO3↓+2NaCl的离子方程式分析;
D.写出CaCl2+Na2CO3═CaCO3↓+2NaCl的离子方程式分析.
B.属于复分解反应;
C.写出CaCl2+Na2CO3═CaCO3↓+2NaCl的离子方程式分析;
D.写出CaCl2+Na2CO3═CaCO3↓+2NaCl的离子方程式分析.
解答:
解:A.Ca2++CO32-═CaCO3↓,反应中没有元素化合价的变化,不属于氧化还原反应,也不是化合反应,故A错误;
B.Ca2++CO32-═CaCO3↓属于复分解反应,没有元素化合价的变化,属于非氧化还原反应,故B正确;
C.CaCl2+Na2CO3═CaCO3↓+2NaCl的离子方程式为:Ca2++CO32-═CaCO3↓,故C正确;
D.CaCl2+Na2CO3═CaCO3↓+2NaCl的离子方程式为Ca2++CO32-═CaCO3↓,故D正确.
故选A.
B.Ca2++CO32-═CaCO3↓属于复分解反应,没有元素化合价的变化,属于非氧化还原反应,故B正确;
C.CaCl2+Na2CO3═CaCO3↓+2NaCl的离子方程式为:Ca2++CO32-═CaCO3↓,故C正确;
D.CaCl2+Na2CO3═CaCO3↓+2NaCl的离子方程式为Ca2++CO32-═CaCO3↓,故D正确.
故选A.
点评:本题考查了氧化还原反应、离子反应、复分解反应等,侧重于反应类型的判断的考查,题目难度不大.

练习册系列答案
相关题目
有关化学资源的合成、利用与开发的叙述合理的是( )
| A、大量使用化肥和农药,能不断提高农作物产量 |
| B、通过有机合成,可以制造出比钢铁更强韧的新型材料 |
| C、安装煤炭燃烧过程的“固硫”装置,主要是为了提高煤的利用率 |
| D、开发利用可燃冰(固态甲烷水合物),有助于海洋生态环境的治理 |
下列物质之间反应,不可能发生爆炸的是( )
| A、H2与F2 |
| B、H2与I2 |
| C、H2与O2 |
| D、Na与S |
下列说法正确的是( )
| A、弱碱溶于水后能促进水的电离 |
| B、盐溶于水后一定能促进水的电离 |
| C、任何条件下,只要pH>7,溶液就一定显碱性 |
| D、任何条件下,只要c(H+)>c(OH-),溶液就一定显酸性 |
如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面图.下列说法正确的是( )
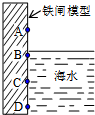

| A、该电化腐蚀为析氢腐蚀 |
| B、图中生成铁锈最多的是C区域 |
| C、A区域比B区域更易腐蚀 |
| D、铁闸中的负极的电极反应:Fe-2e-=Fe2+ |
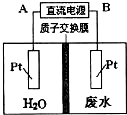 用如图所示装置处理含NO3-的酸性工业废水,某电极反应式为2NO3-+12H++10e-=N2+6H2O,则下列说法错误的( )
用如图所示装置处理含NO3-的酸性工业废水,某电极反应式为2NO3-+12H++10e-=N2+6H2O,则下列说法错误的( )| A、电源正极为A,电解过程中有气体放出 |
| B、电解时H+从质子交换膜左侧向右侧移动 |
| C、电解过程中,右侧电解液pH保持不变 |
| D、电解池一侧生成5.6g N2,另一侧溶液质量减少l8g |
某一化学反应在不同条件下的能量变化曲线如图所示.下列说法正确的是( )
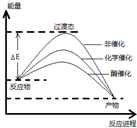

| A、化学催化比酶催化的效果好 |
| B、使用不同催化剂可以改变反应的能耗 |
| C、反应物的总能量低于生成物的总能量 |
| D、使用不同催化剂可以改变反应的热效应 |
下列有关化学用语正确的是( )
A、Cl-离子的结构示意图: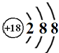 |
B、次氯酸的电子式 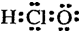 |
C、丙烷分子的比例模型示意图: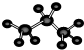 |
D、甲烷的结构式为: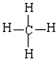 |