��Ŀ����
17����ҵ���������β���к��е�������NOx��NO��NO2�Ļ������費��N2O4��������̬���������ཡ�������ϴ����в����1����ҵ�Ͽ��ð������շ�����NOx����Ӧԭ�����£�
4xNH3+6NOx $\frac{\underline{\;����\;}}{\;}$��2x+3��N2+6xH2O
ij��ѧ��ȤС��ģ��ô������̵�ʵ��װ�����£�
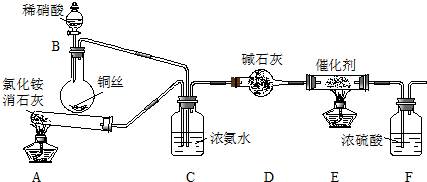
��װ��A�з�����Ӧ�Ļ�ѧ����ʽΪ2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��
��װ��C��������ʹNH3��NO��Ͼ��Ȳ������������٣�
��װ��F������������ĩ��Ӧ��NH3��ֹ��Ⱦ������
��2����ҵ��Ҳ����Na2CO3��Һ���շ�����NOx��
��֪��NO������Na2CO3��Һ��Ӧ����
NO+NO2+Na2CO3=2NaNO2+CO2 ��I��
2NO2+Na2CO3=NaNO2+NaNO3+CO2 ��II��
�ٵ�NOx��Na2CO3��Һ��ȫ����ʱ��x��ֵ��������A������ĸ����
A��1.3 B��1.6 C��1.8
�ڽ�1mol NOx ͨ��Na2CO3��Һ�У�����ȫ����ʱ����Һ�����ɵ�NO3����NO2���������ӵ����ʵ�����x�仯��ϵ��ͼ��ʾ��

ͼ���߶�a��ʾNO2-������xֵ�仯�Ĺ�ϵ������������������Ϊ21.2%�� Na2CO3��Һ���գ�����ҪNa2CO3��Һ����250g��
����������Na2CO3��Һ��ȫ����NOx��ÿ����22.4L����״����CO2��ȫ���ݳ���ʱ������Һ����������44g����NOx�е�xֵΪ1.875��
��3���������շ���Na2CO3��Һ���շ�����NOxβ����ͬ���ŵ��ǽ��ж�����ת��Ϊ�����ʣ���ֹ�ж��������Ⱦ��
���� ��1�����ڼ��������£��Ȼ�狀��������Ʒ�Ӧ�����Ȼ��ơ�������ˮ��
��װ��C�е�Ũ��ˮ����ʹ������Ȼ�ϣ����Կ����������٣�
��װ��F�е�Ũ��������δ��Ӧ�İ�����
��2���ٵ�NOx��Na2CO3��Һ��ȫ����ʱ����n��NO2����n��NO����
�����ü������غ㷨���������
�����ò���������NO��NO2�����ʵ������ٸ���ƽ��Ħ������������xֵ��
��3�����������ж����Ի�������Ⱦ��
��� �⣺��1�����ڼ��������£��Ȼ�狀��������Ʒ�Ӧ�����Ȼ��ơ�������ˮ��2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��
�ʴ�Ϊ��2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��
��װ��C�е�Ũ��ˮ����ʹ������Ȼ�ϣ����Կ����������٣�װ��C��������ʹNH3��NO��Ͼ��Ȳ������������٣�
�ʴ�Ϊ��ʹNH3��NO��Ͼ��Ȳ������������٣�
��װ��F�е�Ũ��������δ��Ӧ�İ�������ֹ����İ����ŷŵ���������Ⱦ������
�ʴ�Ϊ������ĩ��Ӧ��NH3��ֹ��Ⱦ������
��2���ٵ�NOx��Na2CO3��Һ��ȫ����ʱ����n��NO2����n��NO������n��NO2����n��NO��=1ʱxֵ��С��x��СֵΪ$\frac{2+1}{2}$=1.5����Ϊ����NO������x���ֵ��2����x��ȡֵ��ΧΪ1.5��x��2������x��ֵ��������1.3��
�ʴ�Ϊ��A��
���ü�������x=1.5����ӦΪNO��NO2�������ʵ�����Ϊ1��1������ʽ��Ӧ��û��NO3-����aӦ�ñ�ʾNO2-��
���غ㷨����Ӧ���ɵ�NaNO3��NaNO2�е�Ԫ������Ԫ��֮��Ϊ1��1������1mol NOx����ȫ����������̼����0.5mol������Ϊ53g�������̼������Һ������Ϊ250g��
�ʴ�Ϊ��NO2-��250��
������NO2�ʹ��Ӧ����CO2Ϊamol��
��NO��NO2�봿�Ӧ������CO2Ϊbmol��
2NO2+Na2CO3=NaNO2+NaNO3+CO2 ��������
1mol��m=48g
amol 48ag
NO+NO2+Na2CO3=2NaNO2+CO2 ��������
1mol��m=32g
bmol 32bg
a+b=1
48a+32b=44
���a=0.75mol
b=0.25mol
n��NO2��=0.75mol��2+0.25mol=1.75mol
n��NO��=0.25mol
x=$\frac{0.25mol��1+1.75mol��2}{0.25mol+1.75mol}$=1.875��
�ʴ�Ϊ��1.875��
��3�����������ж����Ի�������Ⱦ���ô������յ��������ܽ��ж�����ת��Ϊ�����ʣ���ֹ�ж��������Ⱦ��
�ʴ�Ϊ�����ж�����ת��Ϊ�����ʣ���ֹ�ж��������Ⱦ��
���� �����Ե�������Ϊ���忼�������ʼ�ķ�Ӧ����ȷ���ʵ������ǽⱾ��ؼ����ѵ��ǣ�2����ļ��㣬Ҫ��Ϸ���ʽ�и���������֮��Ĺ�ϵʽ��𣬻���������Ϣ����xֵ���Ѷ��еȣ�

 ��ǰ����ϵ�д�
��ǰ����ϵ�д�| A�� | ��˵��NH3���H+������H2Oǿ��NH3+H3O+=NH4++H2O | |
| B�� | ��˵��������H2O2��Fe3+��2Fe2++H2O2+2H+=2Fe3++2H2O | |
| C�� | ��˵��������ǿ�HCl+AgNO3=AgCl��+HNO3 | |
| D�� | ��˵��CH3COOH��������ʣ�CH3COO-+H2O?CH3COOH+OH- |
| A�� | H2SO4��Ħ��������98g | |
| B�� | 1molO2��������32g | |
| C�� | ����Ħ������������ԭ�ӵ����ԭ������ | |
| D�� | 1molNa+��������23g/mol |
| ʵ�� ��� | ̼��� ״̬ | c��HCl�� /mol•L-1 | ��Һ�¶�/�� | ̼�����ʧ ʱ��/s | |
| ��Ӧǰ | ��Ӧ�� | ||||
| 1 | ��״ | 0.5 | 20 | 39 | 400 |
| 2 | ��ĩ | 0.5 | 20 | 40 | 60 |
| 3 | ��״ | 0.6 | 20 | 41 | 280 |
| 4 | ��״ | 0.8 | 20 | 40 | 200 |
| 5 | ��ĩ | 0.8 | 20 | 40 | 30 |
| 6 | ��״ | 1.0 | 20 | 40 | 120 |
| 7 | ��״ | 1.0 | 30 | 50 | 40 |
| 8 | ��״ | 1.2 | 20 | 40 | 90 |
| 9 | ��״ | 1.2 | 25 | 45 | 40 |
��1������Ӧ���ڷ��ȷ�Ӧ�������Ȼ���ȣ���ʵ���е����з�Ӧ����Ӧǰ����Һ���¶ȱ仯ֵ�����ԼΪ20�棩���Ʋ���ԭ���Ƿ�Ӧ��̼��Ƶ�����ͬ���ų���������ͬ��
��2��ʵ��6��7�������¶ȶԷ�Ӧ������Ӱ�죬�¶�Խ�߷�Ӧ����
Խ�죬�ܱ���ͬһ���ɵ�ʵ�黹��8��9����ʵ����ţ���
��3������ʵ��1��3��4��6��8���Եó������Է�Ӧ���ʵ�Ӱ���������������һ������Ӧ��Ũ��Խ��Ӧ����Խ�죮
��4����ʵ����Ӱ�췴Ӧ���ʵ��������ػ��з�Ӧ��ĽӴ�������ܱ�����һ���ɵ�ʵ�������1��2��4��5��
 �����������壨FeC2O4•2H2O���ʵ���ɫ��ij������Ϊ̽��������������Ļ�ѧ���ʣ�������һϵ��ʵ��̽����
�����������壨FeC2O4•2H2O���ʵ���ɫ��ij������Ϊ̽��������������Ļ�ѧ���ʣ�������һϵ��ʵ��̽������1����ʢ�в�������������Թ��е��뼸�������ữ��KMnO4��Һ����������Һ��ɫ��Ϊ�ػ�ɫ������������̼�������ɣ���˵����������������л�ԭ�ԣ�������ԡ�������ԭ�ԡ����ԡ���������Ӧ������1mol FeC2O4•2H2O����μӷ�Ӧ��KMnO4Ϊ0.6mol��
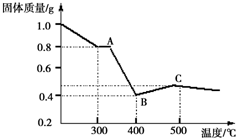
��2�����ϱ��������ܱ������м��ȵ�һ���¶�ʱ�����������������ȫ�ֽ⣬���ɼ��������������Ϊ��ɫ���壮��������ݿα��������ܵ���������������ʣ��Ժ�ɫ��������������¼��裬������ɼ�����ͼ�������
����һ��ȫ����FeO
�������ȫ��������������
��������
��3��Ϊ��֤��������һ�Ƿ��������������������о���
�������о���������ɱ������ݣ�
| ʵ�鲽�裨��Ҫ��д������������̣� | Ԥ��ʵ������ͽ��� |
| ȡ������ɫ���壬��������ϡ�����ϡ���ᣬ����Һ�м������軯����Һ | ��Һ�����ɫ�������һ��������Һ��ɺ�ɫ�������һ������ |
| A�� | +3 | B�� | +4 | C�� | +6 | D�� | +7 |
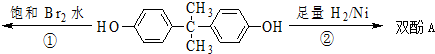
| A�� | ˫��A�ķ���ʽ��C15H16O2 | |
| B�� | ˫��A�ĺ˴Ź���������ʾ��ԭ����֮����1��2��2��3 | |
| C�� | ��Ӧ���У�1 mol˫��A�������4mol Br2 | |
| D�� | ��Ӧ�ڵIJ����������ֹ����� |
| A�� | �Ʊ��屽ʱ����������ˮ��ϣ������� | |
| B�� | ��ȥ�����л��еĶ�����̼ʱ������ͨ���ռ���Һ��Ũ���� | |
| C�� | �����Ը��������Һ�еμӼ��α����������Ϻ�ɫ��ȥ | |
| D�� | �ڱ���ͭ�����Ʊ������� |