题目内容
下列实验问题处理方法正确的是( )
①用pH试纸测溶液pH时,将试纸用水润湿再蘸取待测液
②实验结束后,可将所有的废液倒入下水道排出实验室
③给试管中的液体加热时加入碎瓷片,以免暴沸伤人
④测定硫酸铜结晶水含量时,将晶体加热至白色,然后冷却、称重即可计算
⑤配制稀硫酸时,先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸.
①用pH试纸测溶液pH时,将试纸用水润湿再蘸取待测液
②实验结束后,可将所有的废液倒入下水道排出实验室
③给试管中的液体加热时加入碎瓷片,以免暴沸伤人
④测定硫酸铜结晶水含量时,将晶体加热至白色,然后冷却、称重即可计算
⑤配制稀硫酸时,先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸.
| A、①② | B、③④⑤ |
| C、①③⑤ | D、③⑤ |
考点:化学实验方案的评价
专题:实验评价题
分析:①pH试纸先用水润湿再浸入待测,这样的操作会使溶液变稀;
②根据实验室废液的处理方法进行分析判断;
③根据给试管中的液体加热时的注意事项进行分析判断;
④加热后放在空气中冷却,会吸收空气中的水重新形成晶体;
⑤浓硫酸稀释放出大量的热,且浓硫酸的密度大于水.
②根据实验室废液的处理方法进行分析判断;
③根据给试管中的液体加热时的注意事项进行分析判断;
④加热后放在空气中冷却,会吸收空气中的水重新形成晶体;
⑤浓硫酸稀释放出大量的热,且浓硫酸的密度大于水.
解答:
解:①pH试纸先用水润湿再浸入待测,这样的操作会使溶液变稀,是测量的数据不准确,故①错误;
②实验结束后不能将所有的废液倒入下水道排出实验室,以免腐蚀下水道、污染环境,故②错误;
③试管内液体若受热不均匀,液体会冲出试管,为避免因液体冲出伤人,故要不时移动试管或加入碎瓷片,故③正确;
④加热后放在空气中冷却,会吸收空气中的水重新形成晶体,应在干燥器中冷却,故④错误;
⑤因浓硫酸的稀释方法:将浓硫酸沿着器壁(如试管和烧怀壁)慢慢的注入水里,并不断搅拌,使产生的热量迅速地扩散,故⑤正确;
故选D.
②实验结束后不能将所有的废液倒入下水道排出实验室,以免腐蚀下水道、污染环境,故②错误;
③试管内液体若受热不均匀,液体会冲出试管,为避免因液体冲出伤人,故要不时移动试管或加入碎瓷片,故③正确;
④加热后放在空气中冷却,会吸收空气中的水重新形成晶体,应在干燥器中冷却,故④错误;
⑤因浓硫酸的稀释方法:将浓硫酸沿着器壁(如试管和烧怀壁)慢慢的注入水里,并不断搅拌,使产生的热量迅速地扩散,故⑤正确;
故选D.
点评:本题考查化学实验安全及事故处理,难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
酸性高锰酸钾溶液与草酸溶液反应的化学方程式为:2KMnO4+3H2SO4+5H2C2O4═K2SO4+2MnSO4+10CO2↑+8H2O不能使反应速率加大的措施是( )
| A、增大酸性高锰酸钾溶液的浓度 |
| B、增大草酸溶液的浓度 |
| C、增大压强 |
| D、升高温度 |
一定温度下,某密闭容器中发生反应:2SO2(g)+O2?2SO3(g),达到平衡时,n(SO2):n(O2):n(SO3)=2:3:4.保持温度不变,缩小容器体积,反应再次达到平衡时,O2和SO3的物质的量分别为0.8mol、1.4mol,此时SO2的物质的量应是( )
| A、0.2mol |
| B、0.4mol |
| C、0.8mol |
| D、1.0mol |
某一元醛发生银镜反应,生成金属银4.32g,等量该醛完全燃烧后,可生成水1.08g.则此醛可以是下列中的( )
| A、丙醛 | B、丙烯醛 | C、丁醛 | D、乙醛 |
下列关于使用托盘天平的叙述,不正确的是( )
| A、称量前先调节托盘天平的零点 |
| B、称量时左盘放被称量物,右盘放砝码 |
| C、潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量 |
| D、用托盘天平可以准确称量至0.01g |
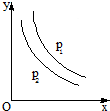 反应:aL(s)+bG(g)?cR(g)达到平衡,温度和压强对该反应的影响如下图所示,图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气体中G的体积分数.据此可判断( )
反应:aL(s)+bG(g)?cR(g)达到平衡,温度和压强对该反应的影响如下图所示,图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气体中G的体积分数.据此可判断( )| A、减小压强,混合气体的平均相对分子质量减小 |
| B、上述反应是吸热反应 |
| C、a+b>c |
| D、无法确定a、b的大小 |
 现有含NaCl、MgCl2和Na2SO4的混合溶液,某兴趣小组的同学欲提取纯净的NaCl晶体,设计了如下实验:
现有含NaCl、MgCl2和Na2SO4的混合溶液,某兴趣小组的同学欲提取纯净的NaCl晶体,设计了如下实验: