题目内容
某一元醛发生银镜反应,生成金属银4.32g,等量该醛完全燃烧后,可生成水1.08g.则此醛可以是下列中的( )
| A、丙醛 | B、丙烯醛 | C、丁醛 | D、乙醛 |
考点:有关有机物分子式确定的计算
专题:
分析:根据关系式-CHO~2Ag,根据生成金属银的质量可以求得醛的物质的量,然后根据生成水的质量结合氢原子守恒可以获得H的个数,确定分子式即可.
解答:
解:4.32g银物质的量n=
=
=0.04mol,根据关系式-CHO~2Ag,故一元醛为0.02mol.醛完全燃烧时,生成的水为1.08g,即n=
=
=0.06mol,含H为0.12mol.则该醛分子中有6个氢原子,
A.丙醛CH3CH2CHO,故A正确;
B.丙烯醛CH2=CHCHO,故B错误;
C.丁醛CH3CH2CH2CHO,故C错误;
D.乙醛CH3CHO,故D错误;
故选A.
| m |
| M |
| 4.32g |
| 108g/mol |
| m |
| M |
| 1.08g |
| 18g/mol |
A.丙醛CH3CH2CHO,故A正确;
B.丙烯醛CH2=CHCHO,故B错误;
C.丁醛CH3CH2CH2CHO,故C错误;
D.乙醛CH3CHO,故D错误;
故选A.
点评:本题考查醛的银镜反应,解题关键抓住-CHO~2Ag关系确定醛的物质的量,难度不大.

练习册系列答案
相关题目
下列与有机物结构、性质相关的叙述正确的是( )
| A、乙醇分子和水分子中都含有羟基,均可与金属钠反应生成氢气 |
| B、苯和乙烯分别与酸性高锰酸钾溶液混合,现象相同 |
| C、淀粉和纤维素均为多糖,属于同分异构体 |
| D、石油的分馏、煤的干馏、煤的气化和液化均为物理变化 |
一定条件下将2mol SO2和2mol SO3气体混合于一固定容积的密闭容器中,发生反应:2SO2+O2?2SO3,平衡时SO3为n mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是( )
| A、2 mol SO2+1 mol O2 |
| B、4 mol SO2+1 mol O2 |
| C、2 mol SO2+1 mol O2+2 SO3 |
| D、3 mol SO2+1 mol O2+1 SO3 |
单质铁溶于一定浓度的硝酸溶液中反应的离子方程式为:aFe+bNO3-+cH+=dFe2++fFe3++gNO↑+hNO2↑+kH2O.下列关系一定成立的是( )
| A、2d+3f-b+c=0 |
| B、2d+3f-3g-h=0 |
| C、4b-2h-c=0 |
| D、若d:f=1,则g:h=1 |
下列实验问题处理方法正确的是( )
①用pH试纸测溶液pH时,将试纸用水润湿再蘸取待测液
②实验结束后,可将所有的废液倒入下水道排出实验室
③给试管中的液体加热时加入碎瓷片,以免暴沸伤人
④测定硫酸铜结晶水含量时,将晶体加热至白色,然后冷却、称重即可计算
⑤配制稀硫酸时,先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸.
①用pH试纸测溶液pH时,将试纸用水润湿再蘸取待测液
②实验结束后,可将所有的废液倒入下水道排出实验室
③给试管中的液体加热时加入碎瓷片,以免暴沸伤人
④测定硫酸铜结晶水含量时,将晶体加热至白色,然后冷却、称重即可计算
⑤配制稀硫酸时,先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸.
| A、①② | B、③④⑤ |
| C、①③⑤ | D、③⑤ |
除去FeCl2溶液中FeCl3和CuCl2杂质可选用( )
| A、NaOH |
| B、Cl2水 |
| C、Fe粉 |
| D、Mg粉 |
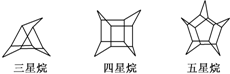 化学家们合成了如图所示的一系列的星烷.下列说法正确的是( )
化学家们合成了如图所示的一系列的星烷.下列说法正确的是( )| A、它们的一氯代物均只有三种 |
| B、它们之间互为同系物 |
| C、三星烷与乙苯互为同分异构体 |
| D、六星烷的化学式为C18H24 |