题目内容
原电池中发生的化学反应属于 ,原电池将 能转变为 能.其中,电子流出的一极是原电池的 极,该极发生 反应,电子流入的一极是原电池的 极,该极发生 反应.原电池中电解质溶液的作用是 .
考点:原电池和电解池的工作原理
专题:电化学专题
分析:依据原电池工作原理解答:原电池是将氧化还原反应分成两个半反应,分别在两个电极发生,将化学能转化为电能的装置,原电池负极为电子流出极,发生氧化反应,正极为电子流入极,发生还原反应,外电路电子在导线中定向移动,内电路中电解质中的阴阳离子定向移动,形成闭合回路,据此解答.
解答:
解:原电池是将氧化还原反应分成两个半反应,分别在两个电极发生,将化学能转化为电能的装置,原电池负极为电子流出极,发生氧化反应,正极为电子流入极,发生还原反应,外电路电子在导线中定向移动,内电路中电解质中的阴阳离子定向移动,形成闭合回路;
故答案为:氧化还原反应;化学;电;负;氧化;正;还原;使溶液导电,形成闭合回路.
故答案为:氧化还原反应;化学;电;负;氧化;正;还原;使溶液导电,形成闭合回路.
点评:本题考查了原电池工作的原理,题目难度不大,侧重考查学生对基础知识的掌握.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
当光束通过下列分散系时,能观察到丁达尔现象的是( )
| A、NaCl溶液 |
| B、Na2CO3溶液 |
| C、Na2SO4溶液 |
| D、Fe(OH)3胶体 |
下列实验问题处理方法正确的是( )
①用pH试纸测溶液pH时,将试纸用水润湿再蘸取待测液
②实验结束后,可将所有的废液倒入下水道排出实验室
③给试管中的液体加热时加入碎瓷片,以免暴沸伤人
④测定硫酸铜结晶水含量时,将晶体加热至白色,然后冷却、称重即可计算
⑤配制稀硫酸时,先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸.
①用pH试纸测溶液pH时,将试纸用水润湿再蘸取待测液
②实验结束后,可将所有的废液倒入下水道排出实验室
③给试管中的液体加热时加入碎瓷片,以免暴沸伤人
④测定硫酸铜结晶水含量时,将晶体加热至白色,然后冷却、称重即可计算
⑤配制稀硫酸时,先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸.
| A、①② | B、③④⑤ |
| C、①③⑤ | D、③⑤ |
石油中常会有少量硫醇,因而产生难闻气味.硫醇是巯基(-SH)与链烃基相连的含硫化合物,其性质与醇类有相似之处.但是,由于巯基的存在,也导致硫醇有一些醇类所没有的化学性质,例如,硫醇能跟NaOH溶液反应生成盐,硫醇在空气中能被氧化等等.根据信息,判断下列关于硫醇性质的比较,正确的是( )
| A、沸点:C2H5SH>C3H7SH |
| B、还原性:C2H5SH>C2H5OH |
| C、水溶性:C2H5SH>C2H5OH |
| D、酸性:C2H5SH<C2H5OH |
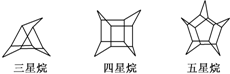 化学家们合成了如图所示的一系列的星烷.下列说法正确的是( )
化学家们合成了如图所示的一系列的星烷.下列说法正确的是( )| A、它们的一氯代物均只有三种 |
| B、它们之间互为同系物 |
| C、三星烷与乙苯互为同分异构体 |
| D、六星烷的化学式为C18H24 |
分子式为CNH2NO2的羧酸和某醇酯化生成分子式为CN+2H2N+4O2的酯,反应所需羧酸和醇的质量比为1:1,则该羧酸是( )
| A、乙酸 | B、丙酸 | C、甲酸 | D、乙二酸 |
下列各组离子一定能大量共存的是( )
| A、在含有大量[Al(OH)4]-溶液中NH4+、Na+、Cl-、H+ |
| B、在强碱溶液中 Na+、K+、CO32-、NO3- |
| C、在pH=12的溶液中 NH4+、Na+、SO42-、Cl- |
| D、在c(H+)=0.1 mol?L-1的溶液中K+、I-、Cl-、NO3- |
设NA为阿伏加德罗常数的值,下列说法中,正确的是( )
| A、2.4 g金属镁所含电子数目为0.2 NA |
| B、1 mol H2SO4所含粒子数目为NA |
| C、17 g NH3所含中子数目为10 NA |
| D、18 g水所含分子数目为NA |
 食品保鲜膜是老百姓的日常家用品.食品保鲜膜按材质分为聚乙烯(PE)、聚氯乙烯(PVC)、聚偏二氯乙烯(PVDC)等种类.PVC被广泛地用于食品、蔬菜外包装,它对人体有潜在危害.化学工作者十分关注聚氯乙烯(PVC)保鲜膜的安全问题.PVC保鲜膜的安全隐患主要来自于塑料中残留的PVC单体以及不符合国家标准的增塑剂DEHA.回答下列问题:
食品保鲜膜是老百姓的日常家用品.食品保鲜膜按材质分为聚乙烯(PE)、聚氯乙烯(PVC)、聚偏二氯乙烯(PVDC)等种类.PVC被广泛地用于食品、蔬菜外包装,它对人体有潜在危害.化学工作者十分关注聚氯乙烯(PVC)保鲜膜的安全问题.PVC保鲜膜的安全隐患主要来自于塑料中残留的PVC单体以及不符合国家标准的增塑剂DEHA.回答下列问题: