题目内容
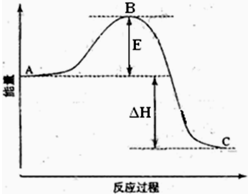 2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下列问题:
2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下列问题:(1)图中A、C分别表示
(2)图中△H=
考点:反应热和焓变
专题:化学反应中的能量变化
分析:(1)反应物总能量大于生成物总能量,为放热反应,加入催化剂,活化能减小,反应反应热不变;
(2)根据反应2SO2(g)+O2(g)=2SO3(g)结合1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1计算反应热.
(2)根据反应2SO2(g)+O2(g)=2SO3(g)结合1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1计算反应热.
解答:
解:(1)因图中A、C分别表示反应物总能量、生成物总能量,E为活化能,反应热可表示为A、C活化能的大小之差,活化能的大小与反应热无关,加入催化剂,活化能减小,反应反应热不变;
故答案为:反应物能量;生成物能量;无;降低;不变;因为催化剂改变了反应的历程使活化能E降低,但不能改变反应物的总能量和生成物的总能量之差,不改变反应热;
(2)因1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1,所以2molSO2(g)氧化为2molSO3的△H=-198kJ?mol-1,
则2SO2(g)+O2(g)=2SO3(g)△H=-198KJ?mol-1,故答案为:-198.
故答案为:反应物能量;生成物能量;无;降低;不变;因为催化剂改变了反应的历程使活化能E降低,但不能改变反应物的总能量和生成物的总能量之差,不改变反应热;
(2)因1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1,所以2molSO2(g)氧化为2molSO3的△H=-198kJ?mol-1,
则2SO2(g)+O2(g)=2SO3(g)△H=-198KJ?mol-1,故答案为:-198.
点评:本题综合考查反应热与焓变,为高考常见题型,侧重于学生的分析能力和计算能力的考查,注意催化剂对反应的影响以及反应热计算的应用,题目较简单.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
关于反应11P+15CuSO4+24H2O→5Cu3P+6H3PO4+15H2SO4,下列说法正确的是( )
| A、P仅作还原剂,其氧化产物是H3PO4 |
| B、每转移3mol电子,有0.6mol P被氧化 |
| C、15molCuSO4可氧化6molP |
| D、该反应的氧化剂与还原剂的物质的量之比为5:6 |
对于以下的反应过程,一定要加入氧化剂才能够实现的是( )
| A、O2→H2O |
| B、SO2→SO42- |
| C、H2SO4→CuSO4 |
| D、HNO3→NO2 |
能正确表示下列反应的离子反应方程式为( )
| A、NH4HCO3溶液与过量的KOH溶液反应:NH4++HCO3-+2OH-=CO32-+NH3↑+2H2O |
| B、向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -=2Al(OH)3↓+3BaSO4↓ |
| C、向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
| D、醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O |


