题目内容
(一)下图是工业开发海水的某工艺流程.

(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽,离子膜和隔膜均允许通过的分子或离子是 ;电解槽中的阳极材料为 .
(2)本工艺流程中先后制得Br2、CaSO4和Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4顺序制备?
答: ;原因是 .
(3)溴单质在四氯化碳中的溶解度比在水中大得多,四氯化碳与水不互溶,故可用于萃取溴,但在上述工艺中却不用四氯化碳,原因是 .
(二)为配制某培养液需要NaH2PO4和Na2HPO4(物质的量比为3:1)的混合液,每升混合液中含磷元素3.1g.现用4.0mol?L-1 H3PO4溶液和固体NaOH配制2.0L该混合液.
(1)写出相关反应的化学方程式 、 .
(2)需取NaOH的质量为 克.

(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽,离子膜和隔膜均允许通过的分子或离子是
(2)本工艺流程中先后制得Br2、CaSO4和Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4顺序制备?
答:
(3)溴单质在四氯化碳中的溶解度比在水中大得多,四氯化碳与水不互溶,故可用于萃取溴,但在上述工艺中却不用四氯化碳,原因是
(二)为配制某培养液需要NaH2PO4和Na2HPO4(物质的量比为3:1)的混合液,每升混合液中含磷元素3.1g.现用4.0mol?L-1 H3PO4溶液和固体NaOH配制2.0L该混合液.
(1)写出相关反应的化学方程式
(2)需取NaOH的质量为
考点:海水资源及其综合利用,镁、铝的重要化合物,粗盐提纯
专题:实验题
分析:(一)(1)电解饱和食盐水,阳极发生氧化反应,应用石墨为电解,阳极生成氯气,阴极生成氢气和氢氧化钠,则应用阳离子交换膜;
(2)苦卤中加入硫酸,如先加入石灰水,则可生成硫酸钙和氢氧化镁沉淀;
(3)如用四氯化碳萃取,然后还要进行蒸馏操作,操作复杂,且污染环境;
(二)(1)H3PO4可与氢氧化钠反应生成NaH2PO4或Na2HPO4;
(2)2.0L该混合液含有磷元素6.2g,n(P)=
=0.2mol,则反应后n(NaH2PO4)+n(Na2HPO4)=0.2mol,而NaH2PO4和Na2HPO4物质的量比为3:1,则n(NaH2PO4)=0.15mol,n(Na2HPO4)=0.05mol,以此计算n(NaOH)的物质的量,进而计算质量.
(2)苦卤中加入硫酸,如先加入石灰水,则可生成硫酸钙和氢氧化镁沉淀;
(3)如用四氯化碳萃取,然后还要进行蒸馏操作,操作复杂,且污染环境;
(二)(1)H3PO4可与氢氧化钠反应生成NaH2PO4或Na2HPO4;
(2)2.0L该混合液含有磷元素6.2g,n(P)=
| 6.2g |
| 31g/mol |
解答:
解:(一)(1)电解饱和食盐水,电解槽离子膜或隔膜,允许阳离子(或Na+)和水分子通过,不允许阴离子通过;阳极生成氯气,用石墨或钛做电极,
故答案为:阳离子(Na+);钛(或石墨);
(2)工艺流程中先后制得Br2、CaSO4和Mg(OH)2,不能先生成沉淀Mg(OH)2,硫酸钙为微溶物,如果先生成沉淀Mg(OH)2,则沉淀中会夹杂有CaSO4沉淀,使产品不纯,
故答案为:否;如果先沉淀Mg(OH)2,则沉淀中会夹杂有CaSO4沉淀,产品不纯;
(3)因为溴单质在四氯化碳中的溶解度比在水中大得多,而且四氯化碳与水不互溶,因此可用于萃取,但也有缺点,如四氯化碳萃取法工艺复杂、设备投资大;经济效益低、环境污染严重,
故答案为:四氯化碳萃取法工艺复杂、设备投资大,经济效益低、环境污染严重;
(二)(1)H3PO4可与氢氧化钠反应生成NaH2PO4或Na2HPO4,反应的方程式为NaOH+H3PO4=NaH2PO4+H2O、2NaOH+H3PO4=Na2HPO4+2H2O,
故答案为:NaOH+H3PO4=NaH2PO4+H2O;2NaOH+H3PO4=Na2HPO4+2H2O;
(2)2.0L该混合液含有磷元素6.2g,n(P)=
=0.2mol,则反应后n(NaH2PO4)+n(Na2HPO4)=0.2mol,而NaH2PO4和Na2HPO4物质的量比为3:1,则n(NaH2PO4)=0.15mol,n(Na2HPO4)=0.05mol,由钠元素守恒可知需要n(NaOH)=n(NaH2PO4)+2n(Na2HPO4)=0.15mol+0.1mol=0.25mol,
则m(NaOH)=0.25mol×40g/mol=10g,
故答案为:10.
故答案为:阳离子(Na+);钛(或石墨);
(2)工艺流程中先后制得Br2、CaSO4和Mg(OH)2,不能先生成沉淀Mg(OH)2,硫酸钙为微溶物,如果先生成沉淀Mg(OH)2,则沉淀中会夹杂有CaSO4沉淀,使产品不纯,
故答案为:否;如果先沉淀Mg(OH)2,则沉淀中会夹杂有CaSO4沉淀,产品不纯;
(3)因为溴单质在四氯化碳中的溶解度比在水中大得多,而且四氯化碳与水不互溶,因此可用于萃取,但也有缺点,如四氯化碳萃取法工艺复杂、设备投资大;经济效益低、环境污染严重,
故答案为:四氯化碳萃取法工艺复杂、设备投资大,经济效益低、环境污染严重;
(二)(1)H3PO4可与氢氧化钠反应生成NaH2PO4或Na2HPO4,反应的方程式为NaOH+H3PO4=NaH2PO4+H2O、2NaOH+H3PO4=Na2HPO4+2H2O,
故答案为:NaOH+H3PO4=NaH2PO4+H2O;2NaOH+H3PO4=Na2HPO4+2H2O;
(2)2.0L该混合液含有磷元素6.2g,n(P)=
| 6.2g |
| 31g/mol |
则m(NaOH)=0.25mol×40g/mol=10g,
故答案为:10.
点评:本题考查较为综合,涉及海水的综合利用以及溶液的配制等知识,为高频考点,侧重于元素化合物知识的综合理解和运用的考查以及学生的分析能力、实验能力、计算能力的考查,注意把握海水的提取、冶炼原理,把握相关基础知识的积累和学习,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
科学家发现了如下反应:O2+PtF6=O2 (PtF6),其中O2(PtF6)为离子化合物,其中Pt为+5价.下列说法正确的是( )
| A、O2 (PtF6) 中不存在共价键 |
| B、O2 (PtF6)中氧元素的化合价是+l价 |
| C、在此反应中,O2是氧化剂,PtF6是还原剂 |
| D、在此反应中每生成1mol O2 (Pt F6),转移6.02×1023个电子 |
已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为:Cl-<Fe2+<H2O2<I-<SO2,则下列反应不能发生的是( )
| A、2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
| B、I2+SO2+2H2O=H2SO4+2HI |
| C、H2O2+H2SO4=SO2↑+O2↑+2H2O |
| D、2Fe2++Cl2=2Fe3++2Cl- |

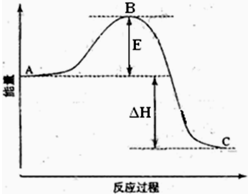 2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下列问题:
2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下列问题: 合成氨工业对国民经济和社会发展具有重要的意义.其原理为:
合成氨工业对国民经济和社会发展具有重要的意义.其原理为:

