��Ŀ����
3����������AlN����һ���������ǽ������ϣ�ijAlN��Ʒ������Al2O3���ʣ�Ϊ�ⶨAlN�ĺ����������������ʵ�鷽������֪��AlN+NaOH+H2O�TNaAlO2+NH3��
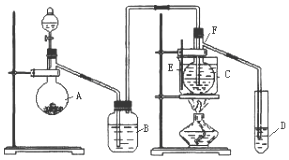
������1��ȡһ��������Ʒ����ͼ1װ�òⶨ��Ʒ��AlN�Ĵ��ȣ��г�װ������ȥ����
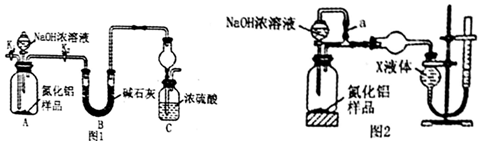
��1����ͼ1��Cװ�������θ���ܵ������Ƿ�ֹ������
��2���������ʵ�鲽�裺��װ��ʵ��װ�ã����ȼ��װ�������ԣ��ټ���ʵ��ҩƷ����������ʵ������ǹر�K1����K2����Һ©������������NaOHŨ��Һ�������ٲ������壮��K1��ͨ�뵪��һ��ʱ�䣬�ⶨCװ�÷�Ӧǰ��������仯��ͨ�뵪����Ŀ���ǰ�װ���в����İ���ȫ������Cװ�ã�
��3������װ�ô���ȱ�ݣ����²ⶨ���ƫ�ߣ�������Ľ����Cװ�ó��ڴ�����һ������װ�ã�
������2����ͼ2װ�òⶨm g��Ʒ��A1N�Ĵ��ȣ����ּг�װ������ȥ����
��4��Ϊ�ⶨ������������������װ���е�XҺ�������ad��������ĸ��ţ�
a��CCl4 b��H2O c��NH4Cl��Һ d��C6H6
��5����m g��Ʒ��ȫ��Ӧ�����������������ΪV mL����ת��Ϊ��״��������AIN����������$\frac{41V}{22400m}$��100%������a�������õ��ɼм�ס�����ѷ�Һ©���Ͽڵ��ܲ���������������ͬ�ϣ������ղⶨ�Ľ����ƫ���ƫ����ƫС������Ӱ�족����
���� ��1�������Ǻ�Ũ�����ܷ�����Ӧ�����壬����������
��2����װ��ʵ��װ�ã�����ԭ����֪�����Ʊ���Ҫ�ȼ��װ�������ԣ�����ʵ��ҩƷ����������ʵ������ǹر�K1����K2����Ӧ���ɰ���������װ���е�����ȫ������װ��C��Ũ�������գ�ȷ�ⶨװ��C�����ؼ��㣻
��3��װ�ô���ȱ���ǿ����е�ˮ�����Ͷ�����̼Ҳ���Խ���װ��C��ʹ�ⶨ���ƫ�ߣ���Ҫ����һ��ʢ��ʯ�Ҹ���ܣ�
��4��������������ˮ������װ���е�XҺ�岻���백����Ӧ������ʹ�����ܽ⣻
��5������AIN+NaOH+H2O�TNaAIO2+NH3���ڶ�����ϵ���㣻�����a����ס����μӵ�Һ�����Ҳ���ų�һ������Һ�壬���Ե��²�õ��������ƫ��
��� �⣺��1����������Ũ�����ܷ�����Ӧ�����壬����������ͼCװ�������θ���ܵ������Ƿ�ֹ���������ã�
�ʴ�Ϊ����ֹ������
��2����װ��ʵ��װ�ã���Ҫ�ȼ��װ�������ԣ�����ʵ��ҩƷ����������ʵ������ǹر�K1����K2����Һ©������������NaOHŨ��Һ�������ٲ������壮��K1��ͨ�뵪��һ��ʱ�䣬�ⶨCװ�÷�Ӧǰ��������仯��ͨ�뵪����Ŀ���ǣ���Ӧ���ɰ���������װ���е�����ȫ������װ��C��Ũ�������գ�ȷ�ⶨװ��C�����ؼ��㣬
�ʴ�Ϊ�����װ�������ԣ��ر�K1����K2����װ���в����İ���ȫ������Cװ�ã�
��3��װ�ô���ȱ���ǿ����е�ˮ�����Ͷ�����̼Ҳ���Խ���װ��C��ʹ�ⶨ���ƫ�ߣ���Ҫ����һ��ʢ��ʯ�Ҹ���ܣ�
�ʴ�Ϊ��Cװ�ó��ڴ�����һ������װ�ã�
��4��a��CCl4�����ܽⰱ���������������Ȼ�̼��Һ�ķ����ⶨ�����������a��ȷ��
b��������������ˮ��������ˮ���ⶨ����b����
c��������������ˮ����������NH4Cl��Һ�ķ����ⶨ�����������c����
d�����������ڱ������������ű���Һ���ⶨ�������������d��ȷ��
�ʴ�Ϊ��ad��
��5����m g��Ʒ��ȫ��Ӧ�����������������ΪV mL����ת��Ϊ��״������
AlN+NaOH+H2O�TNaAIO2+NH3��
41 22.4L
m V��10-3L
m=$\frac{41V��1{0}^{-3}}{22.4}$g����AlN����������=$\frac{41V��1{0}^{-3}}{22.4m}$��100%=$\frac{41V}{22400m}$��100%�������a����ס��װ����ѹǿ�仯��μӵ�Һ�����Ҳ���ų�һ������Һ�壬���Ե��²�õ��������ƫ��
�ʴ�Ϊ��$\frac{41V}{22400m}$��100%��ƫ��
���� ���⿼�������ʺ����IJⶨ̽��ʵ����ƺ�ʵ������жϣ�����ʵ��������������������ǽ���ؼ�����Ŀ�Ѷ��еȣ�ע�����ʵ��ԭ���Լ�����������Ŀ�ģ������ڿ���ѧ����ʵ�������ͼ���������


| A�� | ������ͪ��������2������̼ԭ�� | |
| B�� | ������ˮ��FeCl3��Һ����X��Y | |
| C�� | ���л���X��1H�˴Ź�����ͼ�У���4�������壬1mol X ����������1mol NaOH | |
| D�� | X��Y��������ͪ���ܷ����ӳɡ�ˮ�⡢��������ȥ��Ӧ |
| A�� | �������Բ������п�ʴ���Ƴ�������Ŀ�ĵ��� | |
| B�� | Na2CO3��ĩ��ˮ���ɺ��нᾧˮ��̼���ƾ��壬�þ���һ����Na2CO3•10H2O | |
| C�� | ��ˮ�������������ʹ�ʻ���ɫ | |
| D�� | �Ͻ��Ӳ�ȿ��Դ������Ĵ��������֣��Ͻ���۵�Ҳ���Ե������ijɷֽ��� |
| A�� | �����£���pH=2�������pH=12�İ�ˮ�������ϣ�c��NH4+����c��Cl-����c��OH-����c��H+�� | |
| B�� | 0.1mol•L-1 Na2CO3��Һ��2c��Na+��=c��HCO3-��+c��CO32-��+c��H2CO3�� | |
| C�� | ��ͬ�¶��£�0.6 mol/L��ˮ��Һ��0.3 mol/L��ˮ��Һ��c��OH-��֮����2��1 | |
| D�� | ���ʵ���Ũ����ȵĢ�NH4HSO4��Һ����NH4HCO3��Һ����NH4Cl��Һ�У�c��NH4+���Ĵ�С��ϵ���٣��ڣ��� |
| A�� | 1L 1mol•L-1��������Һ�У������Ȼ��������ΪNA | |
| B�� | 11.2L�����������е�ԭ����ΪNA | |
| C�� | ���³�ѹ��42g��ϩ�Ͷ�ϩ��������У����Լ���Ϊ6NA | |
| D�� | 1L0��lmol/L �� Fe2��SO4��3 ��Һ�У�Fe3+����ĿΪ 0.2NA |
| A�� | �����Ȼ�̼��ȡ��ˮ���²���Һ����ɫ | |
| B�� | �����Ȼ�����Һ�а�ɫ�����������ټ����ᣬ��������ʧ��һ����SO42- | |
| C�� | ���Ȼ�����Һ�м�������������Һ���Ƶ������������� | |
| D�� | ij��Һ�μ���ɫʯ���Լ��ʺ�ɫ������Һһ������ij���� |
 ����14.4gCO��CO2�Ļ�����壬�ڱ�״������ռ�����ԼΪ8.96L���ش��������⣺
����14.4gCO��CO2�Ļ�����壬�ڱ�״������ռ�����ԼΪ8.96L���ش��������⣺