题目内容
15.下列有关实验现象正确的是( )| A. | 用四氯化碳萃取碘水,下层溶液呈紫色 | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 往氯化铁溶液中加入氢氧化钠溶液可制得氢氧化铁胶体 | |
| D. | 某溶液滴加紫色石蕊试剂呈红色,该溶液一定含有某种酸 |
分析 A.四氯化碳的密度比水的密度大,分层,且碘易溶于四氯化碳;
B.白色沉淀可能为AgCl;
C.氯化铁溶液中加入氢氧化钠溶液,发生复分解反应生成沉淀;
D.滴加紫色石蕊试剂呈红色,溶液显酸性.
解答 解:A.四氯化碳的密度比水的密度大,分层,且碘易溶于四氯化碳,则四氯化碳萃取碘水,下层溶液呈紫色,故A正确;
B.白色沉淀可能为AgCl,则原溶液中可能含银离子或硫酸根离子,但二者不能同时存在,故B错误;
C.氯化铁溶液中加入氢氧化钠溶液,发生复分解反应生成沉淀,不能制备胶体,故C错误;
D.滴加紫色石蕊试剂呈红色,溶液显酸性,为酸或强酸的酸式盐、水解显酸性的盐等,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握混合物分离提纯、离子检验、胶体制备、水解与电离等为解答该题的关键,侧重分析与实验能力的考查,注意实验的评价性分析,选项D为易错点,题目难度不大.

练习册系列答案
相关题目
5.下列物质的变化中,能通过一步化学反应完成的是( )
| A. | S→SO3 | B. | Fe→FeCl2 | C. | SiO2→H2SiO3 | D. | Al2O3→Al(OH)3 |
6.实验室欲配制1.00mol/L的NaCl溶液80mL.下列说法正确的是( )
| A. | 选用100mL容量瓶,并用蒸馏水洗净后烘干 | |
| B. | 称取5.9g NaCl固体倒入容量瓶中溶解 | |
| C. | 定容时俯视刻度会导致浓度偏高 | |
| D. | 摇匀、静置后发现凹液面低于刻度线1~2mm,用胶体滴管加水至与刻度线相平即可 |
7.下列判断合理的是( )
①硫酸、烧碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;
②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质;
③碱性氧化物一定是金属氧化物
④根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液;
⑤根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应;
⑥稀释浓H2SO4时,将水慢慢倒入浓H2SO4中,并不断搅拌.
①硫酸、烧碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;
②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质;
③碱性氧化物一定是金属氧化物
④根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液;
⑤根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应;
⑥稀释浓H2SO4时,将水慢慢倒入浓H2SO4中,并不断搅拌.
| A. | 只有②④⑥ | B. | 只有③④⑥ | C. | 只有①③⑤ | D. | 只有①②③⑤ |
6.一定温度下,能说明反应 A(g)+2B(g)?3C(g)已达到平衡状态的是( )
| A. | C 的生成速率与 C 的分解速率相等 | |
| B. | 单位时间内消耗 amolA,同时生成 3amolC | |
| C. | 容器内压强不再变化 | |
| D. | 混合气体的物质的量不再变化 |
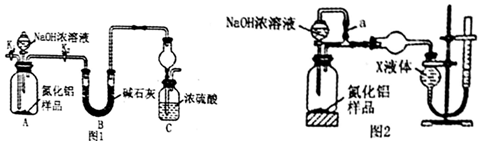

 →
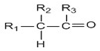
→
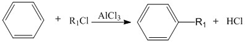
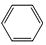 +R1Cl$\stackrel{AlCl_{3}}{→}$
+R1Cl$\stackrel{AlCl_{3}}{→}$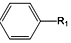 +HCl
+HCl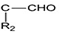 +H2O(R1、R2、R3代表烃基或氢原子)回答下列问题:
+H2O(R1、R2、R3代表烃基或氢原子)回答下列问题: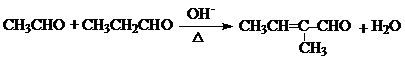 .
.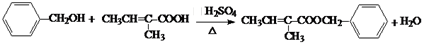 .
.