题目内容
7.下列实验能达到预期目的是( )①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸
②将Cl2的制备和性质实验联合进行,以减少实验中的空气污染
③用食醋和澄清石灰水验证蛋壳中含有碳酸盐
④用溴水检验石油中是否含有乙烯.
| A. | ①②③ | B. | ①③④ | C. | ②③④ | D. | ①②④ |
分析 ①乙醇与乙酸的反应为可逆反应;
②氯气有毒会导致空气污染;
③碳酸钙可以和食醋发生反应生成二氧化碳;
④乙烯能使溴水褪色.
解答 解:①乙醇与乙酸的反应为可逆反应,应用饱和碳酸钠溶液除杂,故①错误;
②氯气有毒会导致空气污染,将Cl2的制备和性质实验联合进行,消耗产生的氯气,可以减少实验中的空气污染,故②正确;
③鸡蛋壳的主要成分碳酸钙可以和食醋发生反应生成二氧化碳,二氧化碳可以使石灰水变浑浊,故③正确;
④乙烯能使溴水褪色,石油是饱和烃,不能使溴水褪色,故④正确;
故选C.
点评 本题考查较为综合,涉及基础实验操作,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验的方法、步骤和使用的仪器,注重相关基础知识的积累,难度不大.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案
相关题目
2.已知:(NH4)2CO3(s)═NH4HCO3(s)+NH3(g)△H=+74.9kJ/mol,下列说法中正确的是( )
| A. | 该反应是熵减小的反应 | |
| B. | 该反应是吸热反应,因此不能自发进行 | |
| C. | 判断反应能否自发进行需要根据△H与△S综合考虑 | |
| D. | (NH4)2CO3(s)比NH4HCO3(s)稳定 |
11.乙烷催化脱氢制取乙烯反应:CH3-CH3(g)?CH2=CH2(g)+H2(g).
(1)上述反应的平衡常数表达式为$\frac{c({H}_{2})c(C{H}_{2}=C{H}_{2})}{c(C{H}_{3}C{H}_{3})}$
(2)下列描述中能说明一定温度下上述反应在恆容容器中已达平衡的是bd.
a.单位时间内生成Amol乙烯同时生成Amol氢气
b.容器中各气体的物质的量不随时间而变化
c.容器中气体密度不随时间而变化
d.容器中气体压强不随时间而变化
(3)已知:
计算上述反应的△H=+128KJ•mol-1.
升高温度,平衡常数K将增大(填“增大”、“减小”或“不变”).
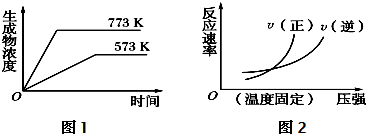
(4)对于上述反应,图1能(“能”或“不能”)表示生成物浓度与温度的关系,理由是温度越高,反应速率越大,达平衡时间越短(或曲线斜率越大);该反应是吸热反应,温度越高,达平衡时生成物浓度越大.图2不能“能”或“不能”)表示反应速率与压强的关系,理由是该反应是气体体积增加的反应,达平衡后再加压,平衡向逆方向移动,V逆>V正.
(5)一定温度下,将n摩尔乙烷放入V升密闭容器中进行催化脱氢,维持容器体积不变,测得乙烷的平衡转化率为a,则该温度下反应的平衡常数K=$\frac{{a}^{2}n}{V(1-a)}$(用含n、V、a的代数式表示).
(1)上述反应的平衡常数表达式为$\frac{c({H}_{2})c(C{H}_{2}=C{H}_{2})}{c(C{H}_{3}C{H}_{3})}$
(2)下列描述中能说明一定温度下上述反应在恆容容器中已达平衡的是bd.
a.单位时间内生成Amol乙烯同时生成Amol氢气
b.容器中各气体的物质的量不随时间而变化
c.容器中气体密度不随时间而变化
d.容器中气体压强不随时间而变化
(3)已知:
| 共价键 | C-C | C=C | C-H | H-H |
| 键能/KJ•mol-1 | 348 | 610 | 413 | 436 |
升高温度,平衡常数K将增大(填“增大”、“减小”或“不变”).
(4)对于上述反应,图1能(“能”或“不能”)表示生成物浓度与温度的关系,理由是温度越高,反应速率越大,达平衡时间越短(或曲线斜率越大);该反应是吸热反应,温度越高,达平衡时生成物浓度越大.图2不能“能”或“不能”)表示反应速率与压强的关系,理由是该反应是气体体积增加的反应,达平衡后再加压,平衡向逆方向移动,V逆>V正.

(5)一定温度下,将n摩尔乙烷放入V升密闭容器中进行催化脱氢,维持容器体积不变,测得乙烷的平衡转化率为a,则该温度下反应的平衡常数K=$\frac{{a}^{2}n}{V(1-a)}$(用含n、V、a的代数式表示).
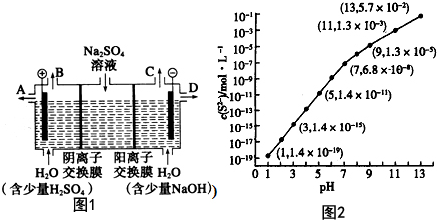
18.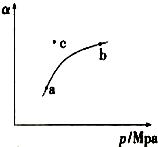 空气质量日报中有一项重要检测指标是SO2的含量,结合所学知识回答下列问题.工业制硫酸的过程中,SO2催化氧化的原理:2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g)△H<0
空气质量日报中有一项重要检测指标是SO2的含量,结合所学知识回答下列问题.工业制硫酸的过程中,SO2催化氧化的原理:2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g)△H<0
(1)某温度下,测得SO2(g)的平衡转化率(α)与体系总压强( p )的关系如上图所示.a、b两点对应的平衡常数K(a)= K(b) (填“>”“<”或“=”,下同)SO3浓度c(a)<c(b) c点,反应速率υ(正)<υ(逆).
(2)将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行,反应得到如下表中的两组数据:
①实验1从开始到反应达到化学平衡时,用去时间t 分钟,则υ(SO2)表示的反应速率为$\frac{1.2}{t}$mol•L-1•min-1 ,②温度T1大于T2的理由是反应放热,温度升高,平衡向左移动,反应物转化率低.
 空气质量日报中有一项重要检测指标是SO2的含量,结合所学知识回答下列问题.工业制硫酸的过程中,SO2催化氧化的原理:2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g)△H<0
空气质量日报中有一项重要检测指标是SO2的含量,结合所学知识回答下列问题.工业制硫酸的过程中,SO2催化氧化的原理:2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g)△H<0(1)某温度下,测得SO2(g)的平衡转化率(α)与体系总压强( p )的关系如上图所示.a、b两点对应的平衡常数K(a)= K(b) (填“>”“<”或“=”,下同)SO3浓度c(a)<c(b) c点,反应速率υ(正)<υ(逆).
(2)将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行,反应得到如下表中的两组数据:
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | ||
| SO2 | O2 | SO2 | O2 | ||
| 1 | T1 | 4 | 2 | x | 0.8 |
| 2 | T2 | 4 | 2 | 0.4 | y |
16.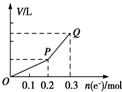 用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定).欲使溶液恢复到起始状态,可向溶液中加入( )
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定).欲使溶液恢复到起始状态,可向溶液中加入( )
 用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定).欲使溶液恢复到起始状态,可向溶液中加入( )
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定).欲使溶液恢复到起始状态,可向溶液中加入( )| A. | 0.1mol CuO | B. | 0.1 mol CuCO3 | ||
| C. | 0.1mol Cu(OH)2 | D. | 0.05 mol Cu2(OH)2CO3 |