题目内容
10.下列反应能用离子方程式OH-+HCO3-→CO32-+H2O表示的是( )| A. | NaOH+NaHCO3→Na2CO3+H2O | |
| B. | Ca(OH)2+Ca(HCO3)2→2CaCO3↓+2H2O | |
| C. | 2NaOH+NH4HCO3→NH3?H2O+Na2CO3+H2O | |
| D. | NaOH+Ca(HCO3)2→2CaCO3↓+H2O+NaHCO3 |
分析 离子方程式OH-+HCO3-→CO32-+H2O表示可溶性强碱与可溶性碳酸氢盐反应生成可溶性碳酸盐和水,依据物质化学式拆分解答.
解答 解:A.NaOH+NaHCO3→Na2CO3+H2O,离子方程式:OH-+HCO3-→CO32-+H2O,故A正确;
B.碳酸钙为沉淀,不能拆,故B错误;
C.反应实质除了氢氧根子与碳酸氢根子外,铵根离子与氢氧根离子也反应,故C错误;
D.碳酸钙为沉淀,应保留化学式,故D错误;
故选:A.
点评 本题考查了离子方程式的书写,明确离子方程式的意义及书写方法是解题关键,注意物质化学式的拆分,题目难度不大.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
18.合金在生活中有广泛应用.下列物质不属于合金的是( )
| A. | 硬铝 | B. | 青铜 | C. | 不锈钢 | D. | 水银 |
15.自2016年1月1日起,无线电动工具中使用的镍镉电池在欧盟全面退市.镍镉电池放电时的总反应为Cd+2NiO(OH)+2H2O═2Ni(OH)2+Cd(OH)2,下列说法正确的是( )
| A. | 电池的电解液为碱性溶液,正极为2NiO(OH)、负极为Cd | |
| B. | 放电时,每通过2 mol电子,负极质量减轻112 g | |
| C. | 放电时,电子从正极流向电源的负极 | |
| D. | 充电时,Cd极板应与外电源的正极相接 |
2.下列叙述不正确的是( )
| A. | 4.6 gNa与O2完全反应,生成7g产物时失去电子的物质的量为0.2 mol | |
| B. | Na与稀硫酸反应的离子方程式为2Na+2H+=2Na++H2↑ | |
| C. | 将少量Na投入到CuSO4溶液中,既有沉淀生成又有气体放出 | |
| D. | 金属钠着火可以用泡沫灭火器或用干燥的沙土灭火 |
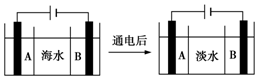 水是一种重要的自然资源,是人类赖以生存不可或缺的物质,水质优劣直接影响人体健康.海水是人类资源宝库,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源.
水是一种重要的自然资源,是人类赖以生存不可或缺的物质,水质优劣直接影响人体健康.海水是人类资源宝库,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源.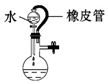
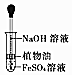
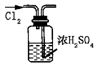

 .它位于元素周期表的第三周期,第ⅢA族.
.它位于元素周期表的第三周期,第ⅢA族.