题目内容
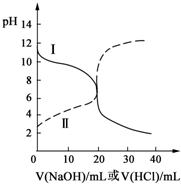 25℃时,取浓度均为0.1mol?L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol?L-1NaOH溶液、0.1mol?L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
25℃时,取浓度均为0.1mol?L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol?L-1NaOH溶液、0.1mol?L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )| A、曲线Ⅰ:滴加溶液到10mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| B、曲线Ⅰ:滴加溶液到20 mL时:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、曲线Ⅱ:滴加溶液在10 mL~20 mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+) |
| D、曲线Ⅱ:滴加溶液到10 mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:根据曲线变化趋势知,当未滴加溶液时,曲线I的pH>7,说明属于酸滴定碱溶液,根据曲线变化趋势知,当未滴加溶液时,曲线II的pH<7,说明属于碱滴定酸溶液;
根据溶液中的溶质及溶液的酸碱性结合电荷守恒来分析解答.
根据溶液中的溶质及溶液的酸碱性结合电荷守恒来分析解答.
解答:
解:根据曲线变化趋势知,当未滴加溶液时,曲线I的pH>7,说明属于酸滴定碱溶液,根据曲线变化趋势知,当未滴加溶液时,曲线II的pH<7,说明属于碱滴定酸溶液;
A.曲线I为酸滴定碱溶液,当滴加溶液到10mL时,溶液中的溶质是氯化铵和一水合氨,溶液呈碱性,则c(H+)<c(OH-),故A错误;
B.曲线I为酸滴定碱溶液,当滴加溶液到20mL时,溶液中的溶质是氯化铵,溶液呈酸性,则c(H+)>c(OH-),溶液中存在电荷守恒c(Cl-)+c(OH-)=c(NH4+)+c(H+),所以得c(Cl-)>c(NH4+),盐类水解程度较小,所以离子浓度大小顺序是c(Cl-)>c(NH4+)>c(H+)>c(OH-),故B正确;
C.曲线II为氢氧化钠滴定醋酸溶液的曲线,滴加溶液在10 mL~20 mL之间,溶液中的溶质是醋酸钠和醋酸,醋酸电离程度大于醋酸根离子水解程度,则溶液中c(H+)>c(OH-),故C错误;
D.滴加溶液到10 mL时,溶液中的溶质是等物质的量浓度的醋酸和醋酸钠,溶液中存在物料守恒c(CH3COO-)+c(CH3COOH)=2c(Na+),溶液中存在电荷守恒c(CH3COO-)+c(H+)=c(OH-)+c(Na+),所以得c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)],故D正确;
故选BD.
A.曲线I为酸滴定碱溶液,当滴加溶液到10mL时,溶液中的溶质是氯化铵和一水合氨,溶液呈碱性,则c(H+)<c(OH-),故A错误;
B.曲线I为酸滴定碱溶液,当滴加溶液到20mL时,溶液中的溶质是氯化铵,溶液呈酸性,则c(H+)>c(OH-),溶液中存在电荷守恒c(Cl-)+c(OH-)=c(NH4+)+c(H+),所以得c(Cl-)>c(NH4+),盐类水解程度较小,所以离子浓度大小顺序是c(Cl-)>c(NH4+)>c(H+)>c(OH-),故B正确;
C.曲线II为氢氧化钠滴定醋酸溶液的曲线,滴加溶液在10 mL~20 mL之间,溶液中的溶质是醋酸钠和醋酸,醋酸电离程度大于醋酸根离子水解程度,则溶液中c(H+)>c(OH-),故C错误;
D.滴加溶液到10 mL时,溶液中的溶质是等物质的量浓度的醋酸和醋酸钠,溶液中存在物料守恒c(CH3COO-)+c(CH3COOH)=2c(Na+),溶液中存在电荷守恒c(CH3COO-)+c(H+)=c(OH-)+c(Na+),所以得c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)],故D正确;
故选BD.
点评:本题考查了酸碱混合溶液定性判断,根据溶液中的溶质及其性质结合电荷守恒和物料守恒来分析解答,题目难度中等.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案
相关题目
某氮的氧化物和CO在催化剂的作用下充分反应,生成氮气和CO2,若测得氮气和CO2的物质的量之比为1:2,则该氮的氧化物是( )
| A、N2O |
| B、N2O5 |
| C、NO2 |
| D、NO |
下列离子方程式正确的是( )
A、乙酸与碳酸钠溶液反应:2H++CO
| ||||
B、油脂在碱性溶液中水解: | ||||
C、苯酚钠溶液中通入二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+
| ||||
D、乙醛溶液与足量的银氨溶液共热CH3CHO+2[Ag(NH3)2]++2OH-
|
一种新型燃料电池,一极通入乙烷,另一极通入氧气,电解质溶液是KOH溶液(足量).下列对此电池的说法正确的是( )
| A、正极反应为:C2H6+18OH--14e-═2CO32-+12H2O |
| B、电池的总反应为:2C2H6+7O2═4CO2+6H2O |
| C、放电一段时间后,正极附近溶液的pH降低 |
| D、每消耗1mol C2H6,电池中就消耗4mol KOH |
铅蓄电池反应原理为:Pb(s)+PbO2(s)+2H2SO4(aq)
2PbSO4(s)+2H2O(l),下列说法正确的是( )
| 放电 |
| 充电 |
| A、放电时,负极的电极反应式为:Pb-2e-═Pb2+ |
| B、放电时,正极得电子的物质是PbO2 |
| C、充电时,电解质溶液中硫酸浓度减小 |
| D、充电时,阴极的电极反应式为:PbSO4-2e-+2H2O═PbO2+4H++SO42- |
下列离子方程式书写正确的是( )
A、把铜片放入浓硫酸中并加热Cu+4H++S
| ||
B、碳酸钙与盐酸反应C
| ||
C、碳酸氢钠溶液和过量盐酸混合HCO
| ||
D、硫酸铜溶液与氢氧化钡溶液反应Ba2++OH-+H++S
|
