题目内容
(1)硫酸氢钾溶液显 性(填“酸”“碱”或“中”),用方程式表示为: ;
(2)碳酸氢钠溶液显 性,用离子方程式表示为
(3)将上述两种溶液混合,现象是 ,反应的离子方程式为 .
(2)碳酸氢钠溶液显
(3)将上述两种溶液混合,现象是
考点:离子方程式的书写,电解质在水溶液中的电离,盐类水解的应用
专题:离子反应专题
分析:(1)硫酸氢钾在溶液中电离出钠离子、氢离子和硫酸根离子,溶液显示酸性;
(2)碳酸氢钠为强电解质,溶液中电离出碳酸氢根离子和钠离子,由于碳酸氢根离子水解,溶液显示碱性;
(3)硫酸氢钾溶液与碳酸氢钠溶液混合后发生反应生成二氧化碳气体.
(2)碳酸氢钠为强电解质,溶液中电离出碳酸氢根离子和钠离子,由于碳酸氢根离子水解,溶液显示碱性;
(3)硫酸氢钾溶液与碳酸氢钠溶液混合后发生反应生成二氧化碳气体.
解答:
解:(1)硫酸氢钾为强电解质,其电离方程式为:KHSO4=K++H++SO42-,所以硫酸氢钾溶液显示酸性,
故答案为:酸;KHSO4=K++H++SO42-;
(2)碳酸氢钠溶液中,碳酸氢根离子离子水解方程式为:HCO3-+H2O=H2CO3+OH-,所以碳酸氢钠显示碱性,
故答案为:碱;HCO3-+H2O=H2CO3+OH-;
(3)硫酸氢钾溶液与碳酸氢钠溶液混合后,会有气泡产生,发生反应的离子方程式为:HCO3-+H+=H2O+CO2↑,
故答案为:有气泡产生;HCO3-+H+=H2O+CO2↑.
故答案为:酸;KHSO4=K++H++SO42-;
(2)碳酸氢钠溶液中,碳酸氢根离子离子水解方程式为:HCO3-+H2O=H2CO3+OH-,所以碳酸氢钠显示碱性,
故答案为:碱;HCO3-+H2O=H2CO3+OH-;
(3)硫酸氢钾溶液与碳酸氢钠溶液混合后,会有气泡产生,发生反应的离子方程式为:HCO3-+H+=H2O+CO2↑,
故答案为:有气泡产生;HCO3-+H+=H2O+CO2↑.
点评:本题考查离子反应方程式的书写、盐的水解原理,为高考常见题型,侧重学生思维严密性的考查,注意把握反应实质及离子反应的书写方法,明确盐的水解原理.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
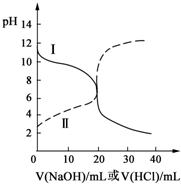 25℃时,取浓度均为0.1mol?L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol?L-1NaOH溶液、0.1mol?L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
25℃时,取浓度均为0.1mol?L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol?L-1NaOH溶液、0.1mol?L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )| A、曲线Ⅰ:滴加溶液到10mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| B、曲线Ⅰ:滴加溶液到20 mL时:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、曲线Ⅱ:滴加溶液在10 mL~20 mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+) |
| D、曲线Ⅱ:滴加溶液到10 mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
下列装置或操作能达到实验目的是( )
A、 分离水和CCl4 |
B、 定容 |
C、 比较两种盐的热稳定性 |
D、 构成铜锌原电池 |
设NA代表阿伏加德罗常数.下列叙述正确的是( )
| A、标准状况下2.24 L H2O中,分子数为0.1NA |
| B、1 L 0.5mol?L-1 AlCl3溶液中含有的Al3+数为0.5 NA |
| C、常温常压下16g O2中,氧原子数为NA |
| D、0.1mol 铁粉与足量的盐酸充分反应,转移的电子数为0.3NA |
浓度均为0.1mol/L的NaOH溶液与氨水相比较,下列结论正确的是( )
| A、NaOH溶液中c(H+)小 |
| B、两溶液中所含的OH-数目相同 |
| C、氨水中c(OH-)大 |
| D、中和HCl的物质的量相同 |
