题目内容
2.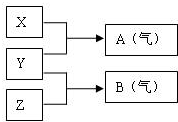 X、Y、Z为三种不同短周期非金属元素的单质.在一定条件下发生如下反应:请针对以下两种不同的情况回答:
X、Y、Z为三种不同短周期非金属元素的单质.在一定条件下发生如下反应:请针对以下两种不同的情况回答:(1)若常温下X、Y、Z均为气体,且A和B在化合生成固体C时有白烟产生,则:
①Y的化学式是H2;
②生成固体C的化学方程式是NH3+HCl=NH4Cl.
(2)若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:
①B的化学式为SO2;
②向苛性钠溶液中通入过量的A所发生反应的离子方程式为H2S+OH-=HS-+H2O;
③将B与某气体单质的水溶液充分反应可生成两种强酸,该反应的化学方程式为SO2+Cl2+2H2O=H2SO4+2HCl.
分析 (1)若常温下X、Y、Z均为气体,A和B化合生成固体C时有白烟产生,应是氯化氢与氨气反应生成氯化铵,则C为NH4Cl,A、B分别为HCl、NH3中的一种,结合转化关系可知Y为H2;
(2)若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,结合转化关系可推知,Y为S、X为H2、A为H2S、B为SO2,以此解答该题.
解答 解:(1)若常温下X、Y、Z均为气体,A和B化合生成固体C时有白烟产生,应是氯化氢与氨气反应生成氯化铵,则C为NH4Cl,A、B分别为HCl、NH3中的一种,结合转化关系可知Y为H2,
①由以上分析可知Y为H2,故答案为:H2;
②生成固体C的化学方程式是:NH3+HCl=NH4Cl,故答案为:NH3+HCl=NH4Cl;
(2)若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,结合转化关系可推知,Y为S、X为H2、A为H2S、B为SO2,
①由以上分析可知B为SO2,故答案为:SO2;
②向苛性钠溶液中通入过量的A,生成NaHS,所发生反应的离子方程式为H2S+OH-=HS-+H2O,故答案为:H2S+OH-=HS-+H2O;
③将B与某气体单质的水溶液充分反应可生成两种强酸,一般可通入氯气,生成硫酸和盐酸,该反应的化学方程式为SO2+Cl2+2H2O=H2SO4+2HCl,
故答案为:SO2+Cl2+2H2O=H2SO4+2HCl.
点评 本题考查无机物推断,为高频考点,侧重考查学生分析推断能力,明确常见元素化合物及其性质是解本题关键,注意某些化学反应产物与反应物的量有关,知道常见元素化合物特殊性质,题目难度不大.

练习册系列答案
相关题目
9.下列过程属于“固氮”的是( )
| A. | 分离液态空气制氮气 | B. | 闪电时N2转化为NO | ||
| C. | 用NH3与CO2合成尿素 | D. | 氨氧化制硝酸 |
6.下列物质的变化,不能通过一步化学反应完成的是( )
| A. | S→SO3 | B. | Fe(OH)2→Fe(OH)3 | C. | N2→NH3 | D. | Na2O2→Na2CO3 |
13.环境问题越来越受到人们的关注,造成环境问题的主要原因大多是由于人类生产活动中过度排放或对自然界物产过度开采引起的.对于下列环境问题的治理不正确的是( )
| A. | 温室效应--减少化石燃料使用,开发清洁能源 | |
| B. | 雾霾--适当限号,减少汽车尾气排放及扬尘 | |
| C. | 白色污染--杜绝生产塑料袋,从根源上治理 | |
| D. | 水体污染--节约用水,减少污水排放 |
7.将充有m mL NO和n mL NO2的量筒倒立于水槽中,然后通入m mL O2,若m<n,则充分反应后,量筒内气体的体积为(单位:mL)( )
| A. | 3(m-n) | B. | m+$\frac{n}{3}$ | C. | $\frac{n-m}{3}$ | D. | $\frac{4n-m}{12}$ |
11.下类物质按酸、碱、盐、氧化物的顺序排列正确的是( )
| A. | 盐酸 纯碱 食盐 氧化铝 | |
| B. | 冰醋酸 烧碱 胆矾 铁红 | |
| C. | 硫酸 熟石灰 漂白粉 过氧化钠 | |
| D. | 王水 氢氧化铝 小苏打 硅胶 |
12.实验测得99℃时,纯水的pH=6.向99℃的纯水中加入适量NaHSO4固体,搅拌使其溶解后恢复到原温度,测得其pH=2.下列说法不正确的是( )
| A. | 99℃时,Kw=l×l0-12 | |
| B. | pH减小的原因是HSO4-离子发生了水解 | |
| C. | 随温度的升高而增大 | |
| D. | 溶液中,水电离出的c(H+)=10-10mol/L |
