题目内容
7.将充有m mL NO和n mL NO2的量筒倒立于水槽中,然后通入m mL O2,若m<n,则充分反应后,量筒内气体的体积为(单位:mL)( )| A. | 3(m-n) | B. | m+$\frac{n}{3}$ | C. | $\frac{n-m}{3}$ | D. | $\frac{4n-m}{12}$ |
分析 发生反应4NO2+O2+2H2O=4HNO3,4NO+3O2+2H2O=4HNO3,故NO与NO2按1:1混合的总反应为:NO+NO2+O2+H2O=2HNO3,充有m mL NO和n mL NO2的量筒倒立于水槽中,然后通入m mL O2,由于m<n,故按总反应进行,NO2有剩余,再发生3NO2+H2O=2HNO3+NO,以此来解答.
解答 解:发生反应4NO2+O2+2H2O=4HNO3,4NO+3O2+2H2O=4HNO3,故NO与NO2按1:1混合的总反应为:NO+NO2+O2+H2O=2HNO3,
充有m mL NO和n mL NO2的量筒倒立于水槽中,然后通入m mL O2,由于m<n,故按总反应进行,NO2有剩余,剩余NO2的体积为n mL-m mL=(n-m)mL,再发生3NO2+H2O=2HNO3+NO,故生成NO的体积为$\frac{1}{3}$(n-m)mL,
故选C.
点评 本题考查混合物的有关计算,为高频考点,侧重于学生的分析、计算能力的考查,题目难度中等,注意利用总方程式进行解答,学生容易进行讨论计算而导致错解.

练习册系列答案
相关题目
13.下列有关物质分类或归类正确的组合有( )
①HDO、双氧水、干冰、碘化银均为化合物
②淀粉、盐酸、水玻璃、氨水均为化合物
③明矾、小苏打、硫酸钡、生石灰均为强电解质
④甲醇、乙二醇、甘油属于同系物
⑤碘酒、牛奶、豆浆、淀粉液均为胶体
⑥H2、D2、T2互为同位素.
①HDO、双氧水、干冰、碘化银均为化合物
②淀粉、盐酸、水玻璃、氨水均为化合物
③明矾、小苏打、硫酸钡、生石灰均为强电解质
④甲醇、乙二醇、甘油属于同系物
⑤碘酒、牛奶、豆浆、淀粉液均为胶体
⑥H2、D2、T2互为同位素.
| A. | 2 个 | B. | 3 个 | C. | 4 个 | D. | 5 个 |
14.把质量相等的Mg分别放在①纯O2中;②空气中;③CO2气体中完全燃烧得到固体的质量分别是W1、W2、W3,三者的大小关系是( )
| A. | W1>W2>W3 | B. | W1=W2=W3 | C. | W3>W1>W2 | D. | W3>W2>W1 |
11.NA表示阿伏伽德罗常数,下列叙述中正确的是( )
| A. | 标准状况下,22.4L水中含有的水分子数为NA | |
| B. | 1mol Fe与足量的盐酸反应电子转移总数为3NA | |
| C. | 常温常压下,22g CO2中含有的氧原子数为NA | |
| D. | 500mL 1mol/L MgCl2溶液中含有Cl-数目为0.5NA |
12. 短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物.n是元素Z 的单质,q是元素X的单质,s是元素Y的单质且常温下为淡黄色固体,m与r相遇会产生白烟.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物.n是元素Z 的单质,q是元素X的单质,s是元素Y的单质且常温下为淡黄色固体,m与r相遇会产生白烟.上述物质的转化关系如图所示.下列说法正确的是( )
 短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物.n是元素Z 的单质,q是元素X的单质,s是元素Y的单质且常温下为淡黄色固体,m与r相遇会产生白烟.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物.n是元素Z 的单质,q是元素X的单质,s是元素Y的单质且常温下为淡黄色固体,m与r相遇会产生白烟.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 单质沸点:W>X>Z | |
| B. | 原子半径:Y>Z>W | |
| C. | Y的氧化物对应的水化物酸性一定比Z的弱 | |
| D. | W、X、Z三种元素组成的化合物一定是共价化合物 |
16.如图所示的实验作,能达到相应目的是( )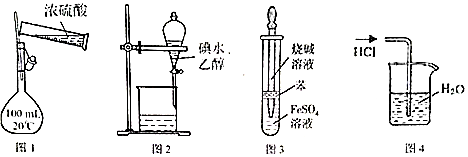

| A. | 用图1装置配制100 mL 0.1mol•L-1硫酸 | |
| B. | 用图2所示装置可萃取碘水中的碘 | |
| C. | 用图3所示装置可制备氢氧化亚铁 | |
| D. | 用图4所示装置可吸收HCl气体 |
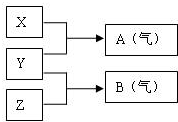 X、Y、Z为三种不同短周期非金属元素的单质.在一定条件下发生如下反应:请针对以下两种不同的情况回答:
X、Y、Z为三种不同短周期非金属元素的单质.在一定条件下发生如下反应:请针对以下两种不同的情况回答: