题目内容
11.下类物质按酸、碱、盐、氧化物的顺序排列正确的是( )| A. | 盐酸 纯碱 食盐 氧化铝 | |
| B. | 冰醋酸 烧碱 胆矾 铁红 | |
| C. | 硫酸 熟石灰 漂白粉 过氧化钠 | |
| D. | 王水 氢氧化铝 小苏打 硅胶 |
分析 根据物质类别的概念可知,酸是由氢离子和酸根离子构成,碱是由金属阳离子和氢氧根离子构成,盐是由金属离子和酸根离子构成,氧化物中只有两种元素且含有氧元素,据此逐一判断.
解答 解:A.盐酸是氯化氢水溶液,是混合物,纯碱是碳酸钠属于盐,故A错误;
B.冰醋酸为纯净的乙酸,属于酸,烧碱是氢氧化钠属于碱,胆矾是五水合硫酸铜的俗称,其化学式为:CuSO4•5H2O,属于盐,铁红为氧化铁,其化学式为:Fe2O3,属于氧化物,故B正确;
C.工业用氯气和冷的消石灰反应制备漂白粉,发生2Ca(OH)2+2Cl2=CaCl2+H2O+Ca(ClO)2,成分为CaCl2、Ca(ClO)2,故C错误;
D.王水是浓盐酸(HCl)和浓硝酸(HNO3)组成的混合物,属于混合物,硅酸凝胶经干燥脱水形成的硅酸干胶称为硅胶,主要成分是硅酸,不属于氧化物,故D错误;
故选B.
点评 本题考查物质类别的分析,学生应能利用物质的组成和性质来分析物质的类别,并熟悉常见物质的分类来解答,题目难度不大.

练习册系列答案
相关题目
17.在800℃时,当反应CO(g)+H2O(g)?CO2(g)+H2(g)在密闭容器中达到平衡后,CO、H2O(g)、CO2、H2的物质的量都是1mol,如果在此容器中再通入3mol水蒸气,则重新达到平衡后,其中CO2的物质的量可能是( )
| A. | 1.43mol | B. | 2mol | C. | 0.8mol | D. | 1mol |
6.在一定体积的密闭容器中,进行如下化学反应:其化学平衡常数K与温度t的关系如下:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
请回答下列问题:
(1)该反应为吸热反应.(填“吸热”或“放热”)
(2)830℃,固定容器为2L的密闭容器中,放入混合物,其始浓度为c(CO)=0.1mol/L,c(H2O)=0.3mol/L,经3s后达到平衡;则平衡时CO的物质的量为;3s内CO2的平均反应速率为0.025mol/(L•s).
(3)可以判断已知的可逆反应达到平衡状态的是c(填字母代号).
a.容器内的压强不再变化
b.单位时间内生成amolCO2同时消耗amolCO
c.容器内生成的CO浓度与H2浓度相等
d.单位时间内生成amolCO2同时生成2amolCO
e.单位时间内生成amolCO2同时生成amolH2.
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应为吸热反应.(填“吸热”或“放热”)
(2)830℃,固定容器为2L的密闭容器中,放入混合物,其始浓度为c(CO)=0.1mol/L,c(H2O)=0.3mol/L,经3s后达到平衡;则平衡时CO的物质的量为;3s内CO2的平均反应速率为0.025mol/(L•s).
(3)可以判断已知的可逆反应达到平衡状态的是c(填字母代号).
a.容器内的压强不再变化
b.单位时间内生成amolCO2同时消耗amolCO
c.容器内生成的CO浓度与H2浓度相等
d.单位时间内生成amolCO2同时生成2amolCO
e.单位时间内生成amolCO2同时生成amolH2.
16.如图所示的实验作,能达到相应目的是( )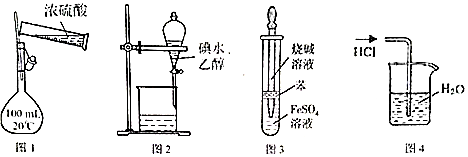

| A. | 用图1装置配制100 mL 0.1mol•L-1硫酸 | |
| B. | 用图2所示装置可萃取碘水中的碘 | |
| C. | 用图3所示装置可制备氢氧化亚铁 | |
| D. | 用图4所示装置可吸收HCl气体 |
3.有关化学基本概念的叙述中,正确的是( )
| A. | 氧化还原反应中一定有元素化合价的升降 | |
| B. | 离子化合物这一定含有金属元素 | |
| C. | 置换反应一定是金属单质与盐酸类之间的反应 | |
| D. | 在常温和101kPa,1mol任何气体的体积约为22.4L |
20.下列试剂的保存方式正确的是( )
| A. | 漂白粉不需要密封保存 | |
| B. | FeCl2溶液保存时加入少量铁粉 | |
| C. | 镁条应保存在煤油中 | |
| D. | NaOH溶液应保存在配有玻璃塞的试剂瓶中 |
1.在卤素中,其最高价氧化物对应水化物的酸性最强的是( )
| A. | F | B. | Cl | C. | Br | D. | I |
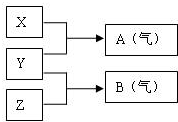 X、Y、Z为三种不同短周期非金属元素的单质.在一定条件下发生如下反应:请针对以下两种不同的情况回答:
X、Y、Z为三种不同短周期非金属元素的单质.在一定条件下发生如下反应:请针对以下两种不同的情况回答: