题目内容
蜂皇酸是蜂王浆的主要活性成分之一,具有灭菌、防辐射、防脱发、抗癌等多种生理功能,蜂皇酸Q只含碳、氢、氧三种元素,其分子中碳、氢、氧原子质量比为120:16:48,经测定Q的相对分子质量不大于200.Q具有酸性,分子中没有支链,1molQ与1molNaOH恰好完全中和,1molQ可以和1molBr2加成.各有机物的转化关系如图所示.
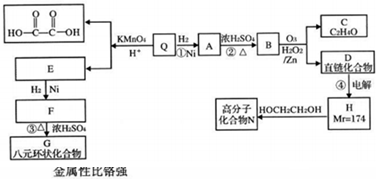
已知R-CH═CH-R′
R-COOH+R′-COOH
R-CH═CH-R′
R-CHO+R′-CHO
(1)写出Q的分子式 ,Q分子中含氧官能团的名称是 .
(2)C的核磁共振氢谱图有2个吸收峰,其面积比为3:1,请写出C与新制氢氧化铜反应的化学方程式: .
(3)在①、②、③、④步反应属于消去反应的是 ,G的结构简式是 .
(4)与D含有相同官能团且分子中只有一个甲基的同分异构体数目为 ,写出其中任意一种结构简式 .
(5)已知在酸性条件下,可采用电解氧化法由D制备有机分子H,则电解D时的阳极反应式是 .
(6)写出H→N化学方程式: .

已知R-CH═CH-R′
| KMnO4/H+ |
R-CH═CH-R′
| O3 |
| H2O2/Zn |
(1)写出Q的分子式
(2)C的核磁共振氢谱图有2个吸收峰,其面积比为3:1,请写出C与新制氢氧化铜反应的化学方程式:
(3)在①、②、③、④步反应属于消去反应的是
(4)与D含有相同官能团且分子中只有一个甲基的同分异构体数目为
(5)已知在酸性条件下,可采用电解氧化法由D制备有机分子H,则电解D时的阳极反应式是
(6)写出H→N化学方程式:
考点:有机物的推断
专题:有机物的化学性质及推断
分析:蜂皇酸Q只含碳、氢、氧三种元素,其分子中碳、氢、氧原子质量比为120:16:48,则分子中C、H、O原子数目之比为
:
:
=12:16:3,Q的分子式可设为(C10H16O3)n,则186n<200,故n=1,Q的分子式即为C10H16O3,由1 mol Q需要1 mol NaOH 完全中和,1 mol Q可以和1 mol Br2 加成,可推知结构中有1个-COOH、1个 ,Q被酸性高锰酸钾氧化生成乙二酸与E,E与氢气发生加成反应生成F,F发生反应生成八元环化合物,应是发生酯化反应,F中含有-COOH、-OH,其-COOH与-OH之间相隔6个碳原子,Q分子中没有支链,综上分析可推出Q含有
,Q被酸性高锰酸钾氧化生成乙二酸与E,E与氢气发生加成反应生成F,F发生反应生成八元环化合物,应是发生酯化反应,F中含有-COOH、-OH,其-COOH与-OH之间相隔6个碳原子,Q分子中没有支链,综上分析可推出Q含有 、-CH=CHCOOH,故Q的结构简式为
、-CH=CHCOOH,故Q的结构简式为 ,则E为
,则E为 ,F为
,F为 ,G为
,G为 .Q与氢气发生加成反应生成A为
.Q与氢气发生加成反应生成A为 ,A发生消去反应生成B,B发生臭氧氧化生成D与C,C的分子式为C2H4O,核磁共振氢谱图有2个吸收峰,其面积比为3:1,故C为CH3CHO,则B为CH3CH=CH(CH2)6COOH,D为OHC(CH2)6COOH,D电解得到H,H相对分子质量比D大16,应是D发生氧化反,故H为HOOC(CH2)6COOH,H与乙二酸发生缩聚反应生成高聚物N为
,A发生消去反应生成B,B发生臭氧氧化生成D与C,C的分子式为C2H4O,核磁共振氢谱图有2个吸收峰,其面积比为3:1,故C为CH3CHO,则B为CH3CH=CH(CH2)6COOH,D为OHC(CH2)6COOH,D电解得到H,H相对分子质量比D大16,应是D发生氧化反,故H为HOOC(CH2)6COOH,H与乙二酸发生缩聚反应生成高聚物N为 ,据此解答.
,据此解答.
| 120 |
| 10 |
| 16 |
| 1 |
| 48 |
| 16 |
 ,Q被酸性高锰酸钾氧化生成乙二酸与E,E与氢气发生加成反应生成F,F发生反应生成八元环化合物,应是发生酯化反应,F中含有-COOH、-OH,其-COOH与-OH之间相隔6个碳原子,Q分子中没有支链,综上分析可推出Q含有
,Q被酸性高锰酸钾氧化生成乙二酸与E,E与氢气发生加成反应生成F,F发生反应生成八元环化合物,应是发生酯化反应,F中含有-COOH、-OH,其-COOH与-OH之间相隔6个碳原子,Q分子中没有支链,综上分析可推出Q含有 、-CH=CHCOOH,故Q的结构简式为
、-CH=CHCOOH,故Q的结构简式为 ,则E为
,则E为 ,F为
,F为 ,G为
,G为 .Q与氢气发生加成反应生成A为
.Q与氢气发生加成反应生成A为 ,A发生消去反应生成B,B发生臭氧氧化生成D与C,C的分子式为C2H4O,核磁共振氢谱图有2个吸收峰,其面积比为3:1,故C为CH3CHO,则B为CH3CH=CH(CH2)6COOH,D为OHC(CH2)6COOH,D电解得到H,H相对分子质量比D大16,应是D发生氧化反,故H为HOOC(CH2)6COOH,H与乙二酸发生缩聚反应生成高聚物N为
,A发生消去反应生成B,B发生臭氧氧化生成D与C,C的分子式为C2H4O,核磁共振氢谱图有2个吸收峰,其面积比为3:1,故C为CH3CHO,则B为CH3CH=CH(CH2)6COOH,D为OHC(CH2)6COOH,D电解得到H,H相对分子质量比D大16,应是D发生氧化反,故H为HOOC(CH2)6COOH,H与乙二酸发生缩聚反应生成高聚物N为 ,据此解答.
,据此解答.解答:
解:蜂皇酸Q只含碳、氢、氧三种元素,其分子中碳、氢、氧原子质量比为120:16:48,则分子中C、H、O原子数目之比为
:
:
=12:16:3,Q的分子式可设为(C10H16O3)n,则186n<200,故n=1,Q的分子式即为C10H16O3,由1 mol Q需要1 mol NaOH 完全中和,1 mol Q可以和1 mol Br2 加成,可推知结构中有1个-COOH、1个 ,Q被酸性高锰酸钾氧化生成乙二酸与E,E与氢气发生加成反应生成F,F发生反应生成八元环化合物,应是发生酯化反应,F中含有-COOH、-OH,其-COOH与-OH之间相隔6个碳原子,Q分子中没有支链,综上分析可推出Q含有
,Q被酸性高锰酸钾氧化生成乙二酸与E,E与氢气发生加成反应生成F,F发生反应生成八元环化合物,应是发生酯化反应,F中含有-COOH、-OH,其-COOH与-OH之间相隔6个碳原子,Q分子中没有支链,综上分析可推出Q含有 、-CH=CHCOOH,故Q的结构简式为
、-CH=CHCOOH,故Q的结构简式为 ,则E为
,则E为 ,F为
,F为 ,G为
,G为 .Q与氢气发生加成反应生成A为
.Q与氢气发生加成反应生成A为 ,A发生消去反应生成B,B发生臭氧氧化生成D与C,C的分子式为C2H4O,核磁共振氢谱图有2个吸收峰,其面积比为3:1,故C为CH3CHO,则B为CH3CH=CH(CH2)6COOH,D为OHC(CH2)6COOH,D电解得到H,H相对分子质量比D大16,应是D发生氧化反,故H为HOOC(CH2)6COOH,H与乙二酸发生缩聚反应生成高聚物N为
,A发生消去反应生成B,B发生臭氧氧化生成D与C,C的分子式为C2H4O,核磁共振氢谱图有2个吸收峰,其面积比为3:1,故C为CH3CHO,则B为CH3CH=CH(CH2)6COOH,D为OHC(CH2)6COOH,D电解得到H,H相对分子质量比D大16,应是D发生氧化反,故H为HOOC(CH2)6COOH,H与乙二酸发生缩聚反应生成高聚物N为 ,
,
(1)有上述分析可知,Q的分子式为C10H16O3,结构简式为 ,所含氧官能团为:羧基、羰基,故答案为:C10H16O3;羧基、羰基;
,所含氧官能团为:羧基、羰基,故答案为:C10H16O3;羧基、羰基;
(2)C为CH3CHO,C与新制氢氧化铜反应的化学方程式: ,
,
故答案为: ;
;
(3)在①、②、③、④步反应,A→B的转化属于消去反应,G的结构简式是 ,故答案为:②;
,故答案为:②; ;
;
(4)D为OHC(CH2)6COOH,与D含有相同官能团且分子中只有一个甲基的同分异构体,以含有-CHO、-COOH为主链,只有一个支链,移动支链确定同分异构体数目,若支链为-CH3,有5种位置,若支链为-CH2CH3,有4种位置,若支链为-CH2CH2CH3,有3种位置,若支链为-CH2CH2CH2CH3,有2种位置,若支链为-CH2CH2CH2CH2CH3,有1种位置,故共有5+4+3+2+1=15种,其中任意一种结构简式为 ,故答案为:15;
,故答案为:15; ;
;
(5)在酸性条件下,可采用电解氧化法由OHC(CH2)6COOH电解制备有机分子HOOC(CH2)6COOH,则电解D时的阳极反应式是:OHC(CH2)6COOH+H2O-2e-=HOOC(CH2)6COOH+2H+,
故答案为:OHC(CH2)6COOH+H2O-2e-=HOOC(CH2)6COOH+2H+;
(6)H→N化学方程式为: ,
,
故答案为: .
.
| 120 |
| 10 |
| 16 |
| 1 |
| 48 |
| 16 |
 ,Q被酸性高锰酸钾氧化生成乙二酸与E,E与氢气发生加成反应生成F,F发生反应生成八元环化合物,应是发生酯化反应,F中含有-COOH、-OH,其-COOH与-OH之间相隔6个碳原子,Q分子中没有支链,综上分析可推出Q含有
,Q被酸性高锰酸钾氧化生成乙二酸与E,E与氢气发生加成反应生成F,F发生反应生成八元环化合物,应是发生酯化反应,F中含有-COOH、-OH,其-COOH与-OH之间相隔6个碳原子,Q分子中没有支链,综上分析可推出Q含有 、-CH=CHCOOH,故Q的结构简式为
、-CH=CHCOOH,故Q的结构简式为 ,则E为
,则E为 ,F为
,F为 ,G为
,G为 .Q与氢气发生加成反应生成A为
.Q与氢气发生加成反应生成A为 ,A发生消去反应生成B,B发生臭氧氧化生成D与C,C的分子式为C2H4O,核磁共振氢谱图有2个吸收峰,其面积比为3:1,故C为CH3CHO,则B为CH3CH=CH(CH2)6COOH,D为OHC(CH2)6COOH,D电解得到H,H相对分子质量比D大16,应是D发生氧化反,故H为HOOC(CH2)6COOH,H与乙二酸发生缩聚反应生成高聚物N为
,A发生消去反应生成B,B发生臭氧氧化生成D与C,C的分子式为C2H4O,核磁共振氢谱图有2个吸收峰,其面积比为3:1,故C为CH3CHO,则B为CH3CH=CH(CH2)6COOH,D为OHC(CH2)6COOH,D电解得到H,H相对分子质量比D大16,应是D发生氧化反,故H为HOOC(CH2)6COOH,H与乙二酸发生缩聚反应生成高聚物N为 ,
,(1)有上述分析可知,Q的分子式为C10H16O3,结构简式为
 ,所含氧官能团为:羧基、羰基,故答案为:C10H16O3;羧基、羰基;
,所含氧官能团为:羧基、羰基,故答案为:C10H16O3;羧基、羰基;(2)C为CH3CHO,C与新制氢氧化铜反应的化学方程式:
 ,
,故答案为:
 ;
;(3)在①、②、③、④步反应,A→B的转化属于消去反应,G的结构简式是
 ,故答案为:②;
,故答案为:②; ;
;(4)D为OHC(CH2)6COOH,与D含有相同官能团且分子中只有一个甲基的同分异构体,以含有-CHO、-COOH为主链,只有一个支链,移动支链确定同分异构体数目,若支链为-CH3,有5种位置,若支链为-CH2CH3,有4种位置,若支链为-CH2CH2CH3,有3种位置,若支链为-CH2CH2CH2CH3,有2种位置,若支链为-CH2CH2CH2CH2CH3,有1种位置,故共有5+4+3+2+1=15种,其中任意一种结构简式为
 ,故答案为:15;
,故答案为:15; ;
;(5)在酸性条件下,可采用电解氧化法由OHC(CH2)6COOH电解制备有机分子HOOC(CH2)6COOH,则电解D时的阳极反应式是:OHC(CH2)6COOH+H2O-2e-=HOOC(CH2)6COOH+2H+,
故答案为:OHC(CH2)6COOH+H2O-2e-=HOOC(CH2)6COOH+2H+;
(6)H→N化学方程式为:
 ,
,故答案为:
 .
.
点评:本题考查有机物推断,综合考查有机化学基础,需要学生对有机化学信息进行利用,解好此类题目的关键是理解和应用好题中所给的信息,综合分析确定Q的结构是关键,再结合转化关系推断,难度较大.

练习册系列答案
相关题目
下列不属于四种基本反应类型,但属于氧化还原反应的是( )
| A、Fe+H2SO4═FeSO4+H2↑ | ||||
B、CO+CuO
| ||||
C、Cu2(OH)2CO3
| ||||
| D、4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
欲配制下列四种无色透明的酸性溶液,其中能配制成功的是( )
| A、NH4+、NO3-、Al3+、Cl- |
| B、Na+、CH3COO-、K+、NO3- |
| C、MnO4-、K+、SO42-、Na+ |
| D、Ca2+、Mg2+、HCO3-、CO32- |
甲溶液的pH=3,乙溶液的pH=6,则下列说法正确的是( )
| A、甲、乙两溶液均呈酸性 |
| B、甲、乙两溶液中c(H+)之比为1:2 |
| C、甲、乙两溶液中水的电离程度大小无法比较 |
| D、甲中水的电离程度小于乙中水的电离程度 |
常温下,把0.1mol?L-1HA溶液(已知其pH=3)和0.05mol?L-1NaOH溶液等体积混合,混合溶液的pH=5,则下列表示混合溶液中粒子浓度关系不正确的是( )
| A、c(A-)>c(Na+) |
| B、c(HA)<c(A-) |
| C、c(Na+)>c(OH-) |
| D、c(HA)+c(A-)=0.1 mol/L |
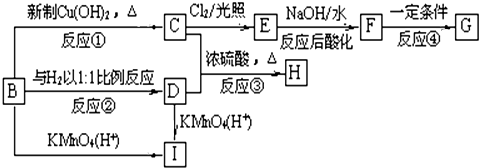
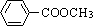 、
、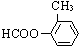 、
、 、
、