题目内容
欲配制下列四种无色透明的酸性溶液,其中能配制成功的是( )
| A、NH4+、NO3-、Al3+、Cl- |
| B、Na+、CH3COO-、K+、NO3- |
| C、MnO4-、K+、SO42-、Na+ |
| D、Ca2+、Mg2+、HCO3-、CO32- |
考点:离子共存问题
专题:离子反应专题
分析:溶液无色,则不存在有颜色的离子,酸性条件下,离子之间不产生气体、沉淀、弱电解质、络合物,不发生氧化还原反应、不发生双水解反应时即可配制成功,以此解答该题.
解答:
解:A.溶液无色,酸性条件下不发生任何反应,可大量给出,能配制成功,故A正确;
B.酸性条件下CH3COO-不能大量存在,故B错误;
C.MnO4-有颜色,不符合题目要求,故C错误;
D.Ca2+、CO32-反应生成沉淀,且酸性条件下,HCO3-、CO32-不能大量存在,故D错误.
故选A.
B.酸性条件下CH3COO-不能大量存在,故B错误;
C.MnO4-有颜色,不符合题目要求,故C错误;
D.Ca2+、CO32-反应生成沉淀,且酸性条件下,HCO3-、CO32-不能大量存在,故D错误.
故选A.
点评:本题以配制溶液为载体考查了离子共存,为高考热点内容,熟悉离子共存的条件及物质的性质是解本题关键,注意隐含条件的挖掘,注意把握离子的性质以及反应类型的判断,为易错点.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
用NA代表阿伏加德罗常数,相关说法不正确的是( )
| A、13.5 g Al与足量盐酸反应生成H2的分子数为NA |
| B、标准状况下,2.24 L CH4所含电子数为NA |
| C、500 mL 1 mol?L-1的K2SO4溶液中含有K+数目为NA |
| D、0.5 mol O2和0.5 mol O3的混合物所含有的氧原子个数为2.5NA |
某溶液中可能含有SO42-、CO32-、Cl-,为了检验其中是否含有SO42-,除BaCl2液外,还需要的溶液是( )
| A、H2SO4 |
| B、HCl |
| C、NaOH |
| D、NaNO3 |
下列说法中正确的是( )
| A、在一定温度和压强下,各种气态物质体积大小由分子间距离决定 |
| B、相同温度时,CO2和N2O若体积相同,则它们的质量一定相同 |
| C、100g浓度为18mol/L的浓硫酸中加入等质量的水稀释浓度大于9mol/L |
| D、14 mol/L的H2SO4溶液的溶质质量分数为80%,那么7 mol/L的H2SO4溶液的溶质质量分数将大于40% |
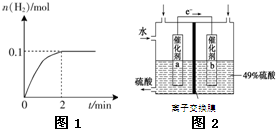 氢能被视为未来的理想清洁能源,科学家预测“氢能”将是21世纪最理想的新能源.目前分解水制氢气的工业制法之一是“硫-碘循环”,主要涉及下列反应:
氢能被视为未来的理想清洁能源,科学家预测“氢能”将是21世纪最理想的新能源.目前分解水制氢气的工业制法之一是“硫-碘循环”,主要涉及下列反应: