题目内容
计算:镁铝混合物共10g,与含1mol HCl的盐酸恰好完全反应.计算混合物中镁铝的物质的量和质量.
考点:有关混合物反应的计算
专题:计算题
分析:设出镁和铝的物质的量,发生的反应方程式有:Mg+2HCl=MgCl2+H2↑、2Al+6HCl=2AlCl3+3H2↑,分别根据总质量、消耗盐酸的物质的量列式计算.
解答:
解:设混合物中含有xmol铝、ymol镁,根据总质量可得:①27x+24y=10,
根据消耗的氯化氢的物质的量及反应方程式Mg+2HCl=MgCl2+H2↑、2Al+6HCl=2AlCl3+3H2↑可得:②3x+2y=1,
联立①②解得:x=
、y=
,
混合物中铝的物质的量为
mol,质量为:27g/mol×
mol=6g,
铝的物质的量为
mol,质量为:24g/mol×
mol=4g,
答:混合物中铝的物质的量为
mol,质量为6g;铝的物质的量为
mol,质量为4g.
根据消耗的氯化氢的物质的量及反应方程式Mg+2HCl=MgCl2+H2↑、2Al+6HCl=2AlCl3+3H2↑可得:②3x+2y=1,
联立①②解得:x=
| 2 |
| 9 |
| 1 |
| 6 |
混合物中铝的物质的量为
| 2 |
| 9 |
| 2 |
| 9 |
铝的物质的量为
| 1 |
| 6 |
| 1 |
| 6 |
答:混合物中铝的物质的量为
| 2 |
| 9 |
| 1 |
| 6 |
点评:本题考查了混合物反应的计算,题目难度不大,明确发生反应的原理为解答关键,试题培养了学生的分析能力及灵活应用基础知识的能力.

练习册系列答案
相关题目
下列离子方程式书写不正确的是( )
A、以石墨作电极电解NaCl溶液:2Cl-+2H2O
| ||||
B、用Pt作电极电解CuSO4溶液:2Cu2++2H2O
| ||||
| C、AlCl3溶液中加入过量稀氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O | ||||
| D、NaAlO2溶液中通入过量的CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
奶粉行业的“911事件”将三聚氰胺引入公众视野,工业上可用尿素为原料,在一定条件下合成三聚氰胺:
6CO(NH2)2→6NH3+3CO2+C3H6N6,对C3H6N6说法正确的是( )
6CO(NH2)2→6NH3+3CO2+C3H6N6,对C3H6N6说法正确的是( )
| A、摩尔质量为126 |
| B、式量为126g?mol-1 |
| C、每个C3H6N6分子含3个N2分子 |
| D、0.1 mol-1C3H6N6含碳原子数为1.806×1023 |
取一定量FeO和Fe2O3的混合物,在H2流中加热充分反应.冷却,称得剩余固体比原混合物质量减少1.200g,若将同量的该混合物与盐酸反应完全,至少需1mol/L盐酸的体积为( )
| A、37.5mL |
| B、75mL |
| C、150mL |
| D、300mL |
最近,美国LawrenceLiremore国家实验室(LLNL)的V.LotA.C?S?Yoo和Cynn成功的在40GPa的高压下,用激光器加热到1800K,将CO2转化为具有类似SiO2结构的原子晶体,其硬度比SiO2还大.下列关于CO2的说法不正确的是( )
| A、CO2是一种酸性氧化物 |
| B、碳氧两种元素只能组成CO2 |
| C、干冰的主要成份是CO2 |
| D、固态CO2的密度比气态CO2的密度大 |
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )


| A、加入Na2SO4可以使溶液由a点变到c点 |
| B、通过蒸发可以使溶液由d点变到c点 |
| C、b点无BaSO4沉淀生成 |
| D、a点对应的Ksp大于c点对应的Ksp |
已知CuS、PbS、HgS的溶度积分别为l.3×l0-36、9.0×10-29、6.4×10-23.下列推断不正确的是( )
| A、硫化钠是处理废水中含上述金属离子的沉淀剂 |
| B、在硫化铅悬浊液中滴几滴硝酸铜溶液,会生成硫化铜 |
| C、在含Hg2+、Cu2+、Pb2+的溶液中滴加硫化钠溶液,当c(S2-)=0.001 mol?L-1时三种金属离子都完全沉淀 |
| D、向含Pb2+、Cu2+、Hg2+的浓度均为0.010 mol?L-1的溶液中通人硫化氢气体,产生沉淀的顺序依次为PbS、CuS、HgS |
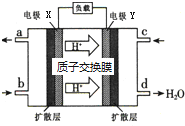 绿色电源“二甲醚-氧气燃料电池”的工作原理如图,
绿色电源“二甲醚-氧气燃料电池”的工作原理如图,