题目内容
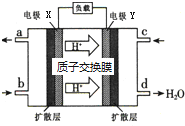 绿色电源“二甲醚-氧气燃料电池”的工作原理如图,
绿色电源“二甲醚-氧气燃料电池”的工作原理如图,(1)氧气应从c处通入,电极Y为
(2)二甲醚(CH3)2O应从b处加入,电极X上发生的电极反应式为
(3)电池在放电过程中,电极X周围溶液的pH
考点:化学电源新型电池
专题:
分析:根据氢离子移动方向知,Y为原电池正极,X为负极,则c处通入的气体是氧气,根据d处生成物知,正极上发生的反应为O2+4e-+4H+═2H2O,电解质溶液为酸性溶液,b处通入的物质是二甲醚,X电极反应式为(CH3)2O-12e-+3H2O=2CO2+12H+,则a处出来的物质是二氧化碳,据此分析解答.
解答:
解:(1)c处通入的气体是氧气,根据d处生成物知,正极上发生的反应为O2+4e-+4H+═2H2O,故答案为:正;O2+4e-+4H+═2H2O;
(2)b处通入的物质是二甲醚,X电极反应式为(CH3)2O-12e-+3H2O=2CO2+12H+,故答案为:(CH3)2O-12e-+3H2O=2CO2+12H+;
(3)电池在放电过程中,电极X发生的电极反应为(CH3)2O-12e-+3H2O=2CO2+12H+,X电极周围溶液的pH减小,故答案为:减小.
(2)b处通入的物质是二甲醚,X电极反应式为(CH3)2O-12e-+3H2O=2CO2+12H+,故答案为:(CH3)2O-12e-+3H2O=2CO2+12H+;
(3)电池在放电过程中,电极X发生的电极反应为(CH3)2O-12e-+3H2O=2CO2+12H+,X电极周围溶液的pH减小,故答案为:减小.
点评:本题考查了化学电源新型电池,根据氢离子移动方向确定正负极,再根据d处生成物确定电解质溶液酸碱性,难点是电极反应式书写,题目难度中等.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
某无色透明溶液中能大量共存的离子组是( )
| A、Na+、Al3+、HCO3-、NO3- |
| B、AlO2-、Mg2+、H+、K+ |
| C、NH4+、Na+、CH3COO-、NO3- |
| D、Na+、NO3-、ClO-、I- |
在下列分类中,前者包含后者的是( )
| A、物质的量、摩尔质量 |
| B、置换反应、氧化还原反应 |
| C、化合物、电解质 |
| D、胶体、分散系 |
镍氢电池是近年开发出来的可充电电池,它可以取代会产生镉污染的镉镍电池.氢镍电池的总反应式是:
H2+NiO(OH)=Ni(OH)2据此反应式判断,下列叙述中正确的是( )
| 1 |
| 2 |
| A、电池放电时,电池负极周围的溶液pH不断增大 |
| B、电池放电时,镍元素被氧化 |
| C、电池放电时,镍元素被还原 |
| D、电池放电时,H2是负极 |
下表是元素周期表的一部分,X、Y、Z、W均为短周期元素,X、Z的质子数之和是2l.下列说法不正确的是( )
| X | Y | ||
| Z | W |
| A、原子半径Z>W>Y |
| B、最高价氧化物对应水化物的酸性Z>W |
| C、氢化物的稳定性X>Z |
| D、X的氢化物与Y的氢化物能发生化合反应生成离子化合物 |
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系;当在某一温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二.

下列分析不正确的是( )

下列分析不正确的是( )
| A、0~4分钟时,A的速率为0.01mol/(L?min) | ||
| B、由T1向T2变化时,V正>V | ||
C、该反应的平衡常数表达式K=
| ||
| D、此反应的正反应为吸热反应. |
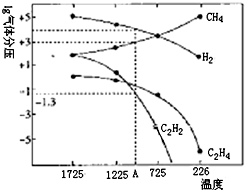 乙炔(C2H2)在气焊、气割及有机合成中用途非常广泛,可由电石(CaC2)直接水化法或甲烷在1500℃左右气相裂解法生产.
乙炔(C2H2)在气焊、气割及有机合成中用途非常广泛,可由电石(CaC2)直接水化法或甲烷在1500℃左右气相裂解法生产.