题目内容
某元素基态原子的最外层电子排布为ns1,当它跟卤素结合时可形成的化学键( )
| A、一定是共价键 |
| B、一定是离子键 |
| C、可能是共价键,也可能是离子键 |
| D、一定是极性共价键 |
考点:原子核外电子排布,化学键
专题:原子组成与结构专题,化学键与晶体结构
分析:某元素基态原子的最外层电子排布为ns1,该元素可能是金属元素也可能是非金属元素(如H),据此判断形成的化学键.
解答:
解:某元素基态原子的最外层电子排布为ns1,该元素可能是金属元素也可能是非金属元素(如H),所以它跟卤素结合时形成化学键可能是共价键HX,也可能是离子键NaX,故C正确.
故选:C.
故选:C.
点评:本题考查了原子的表示法等知识点,难度不大,注意:某元素基态原子的最外层电子排布为ns1,该元素可能是金属元素也可能是非金属元素(如H).

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
将铜和锌用导线连接插入硫酸铜溶液中,当导线中有0.2mol电子通过时,负极质量变化是( )
| A、增加6.5g |
| B、减少6.5g |
| C、减少5.6g |
| D、增加5.6g |
下列说法正确的是 ( )
| A、标况下,1mol任何物质的体积都约为22.4L |
| B、1mol气体的体积约为22.4L |
| C、标况下,1molO2和N2混合气(任意比)的体积约为22.4L |
| D、22.4L气体所含分子数一定大于11.2L气体所含的分子数 |
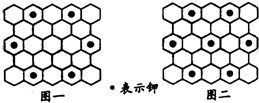 北京大学和中国科学院的化学工作者合作,已成功研制出碱金属与C60形成的石墨夹层离子化合物.将石墨置于熔融的钾或气态的钾中,石墨吸收钾而形成称为钾石墨的物质,其组成可以是C8K、C12K、C24K、C36K、C48K、C60K等等.在钾石墨中,钾原子把价电子交给石墨层,但在遇到与金属钾易反应的其他物质时还会收回.下列分析中正确的是( )
北京大学和中国科学院的化学工作者合作,已成功研制出碱金属与C60形成的石墨夹层离子化合物.将石墨置于熔融的钾或气态的钾中,石墨吸收钾而形成称为钾石墨的物质,其组成可以是C8K、C12K、C24K、C36K、C48K、C60K等等.在钾石墨中,钾原子把价电子交给石墨层,但在遇到与金属钾易反应的其他物质时还会收回.下列分析中正确的是( )| A、题干中所举出的6种钾石墨,属于同素异形体 | ||
| B、若某钾石墨的原于分布如图一所示,则它所表示的是C24K | ||
| C、若某钾石墨的原子分布如图二所示,则它所表示的是C12K | ||
D、另有一种灰色的钾石墨C32K,其中K的分布也类似图中的中心六边形,则最近两个K原子之间的距离为石墨键长的4
|
下列各化合物的命名不正确的是( )
| A、CH2═CH-CH═CH2 1,4-二丁烯 |
B、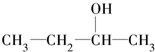 2-丁醇 2-丁醇 |
C、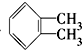 邻二甲苯 邻二甲苯 |
D、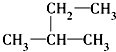 2-甲基丁烷 2-甲基丁烷 |