题目内容
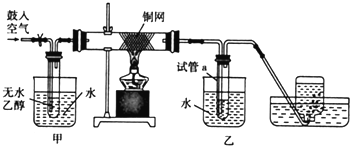
15.化学上常用燃烧法确定有机物组成,这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成.下列装置如图1是用燃烧法确定有机物分子式常用的装置.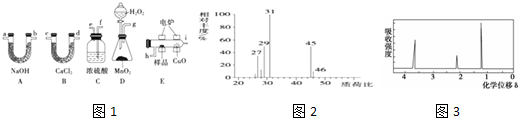
(1)产生的O2按从左到右的流向,所选装置各导管的正确连接顺序是g-f-e-h-i-c-d-a-b.
(2)C装置中浓硫酸的作用是吸水,干燥O2.
(3)D装置中MnO2的作用是催化剂,加快O2的生成.
(4)燃烧管中CuO的作用是使有机物充分氧化生成CO2和H2O.
(5)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.92g样品,经充分反应后,A管质量增加1.76g,B管质量增加1.08g,则该样品的实验式为C2H6O.
(6)用质谱仪测定其相对分子质量,得如图2所示的质谱图,则该有机物的相对分子质量为46.
(7)能否根据A的实验式确定A的分子式能(填“能”或“不能”),若能,则A的分子式是C2H6O(若不能,则此空不填).
(8)该物质的核磁共振氢谱如图3所示,则其结构简式为CH3CH2OH.
分析 A用来吸收二氧化碳、B用来吸收水、C用于干燥通入E中的氧气、D用来制取反应所需的氧气、E是在电炉加热时用纯氧气氧化管内样品,实验时,D中生成的氧气先用浓硫酸干燥,在E中电炉加热下有机物燃烧生成水、二氧化碳,先用氯化钙吸收水,再用氢氧化钠吸收二氧化碳,根据A、B的质量变化可确定生成二氧化碳、水的质量,结合质量守恒确定氧元素的质量,可确定C、H、O的个数比值,以此可确定有机物的实验式,质谱图可确定有机物的相对分子质量,以此可确定有机物分子式,根据核磁共振氢谱可确定有机物含有的H原子种类,以此确定有机物的结构简式,以此解答该题.
解答 解:A用来吸收二氧化碳、B用来吸收水、C用于干燥通入E中的氧气、D用来制取反应所需的氧气、E是在电炉加热时用纯氧气氧化管内样品,实验时,D中生成的氧气先用浓硫酸干燥,在E中电炉加热下有机物燃烧生成水、二氧化碳,先用氯化钙吸收水,再用氢氧化钠吸收二氧化碳,根据A、B的质量变化可确定生成二氧化碳、水的质量,结合质量守恒确定氧元素的质量,可确定C、H、O的个数比值,以此可确定有机物的实验式,质谱图可确定有机物的相对分子质量,以此可确定有机物分子式,根据核磁共振氢谱可确定有机物含有的H原子种类,以此确定有机物的结构简式,
(1)D中生成的氧气中含有水蒸气,应先通过C中的浓硫酸干燥,在E中电炉加热时用纯氧氧化管内样品,生成二氧化碳和水,如有一氧化碳生成,则E中CuO可与CO进一步反应生成二氧化碳,然后分别通入B(吸收水)、A(吸收二氧化碳)中,根据产物的质量推断有机物的组成,则产生的氧气按从左到右流向,所选择装置各导管的连接顺序是g-f-e-h-i-c-d-a-b,
故答案为:g-f-e-h-i-c-d-a-b;
(2)中生成的氧气中含有水蒸气,应先通过C中的浓硫酸干燥,以免影响实验结果,故答案为:吸水,干燥O2;
(3)MnO2为分解制备氧气的催化剂,故答案为:催化剂,加快O2的生成;
(4)一氧化碳能与氧化铜反应,可被氧化成二氧化碳的性质可知,CuO的作用是把有机物不完全燃烧产生的CO转化为CO2;
故答案为:使有机物充分氧化生成CO2和H2O;
(5)A管质量增加1.76g说明生成了1.76g二氧化碳,可得碳元素的质量:1.76g×$\frac{12}{44}$×100%=0.48g,
B管质量增加1.08g说明生成了1.08g水,可得氢元素的质量:1.08g×$\frac{2}{18}$×100%=0.12g,从而可推出含氧元素的质量为:0.92g-0.48g-0.12g=0.32g,
设实验式为CXHYOZ,则X:Y:Z=$\frac{0.48}{12}$:$\frac{0.12}{1}$:$\frac{0.32}{16}$=2:6:1,即实验式为:C2H6O,
故答案为:C2H6O;
(6)由图2可知最大质荷比为46,则有机物的相对分子质量为46,故答案为:46;
(7)该有机物的最简式为C2H6O,H原子已经饱和C原子的四价结构,最简式即为分子式,
故答案为:能;C2H6O;
(8)核磁共振氢谱中给出3种峰,说明该分子中有3种H原子,所以其结构简式为:CH3CH2OH,故答案为:CH3CH2OH.
点评 本题考查用燃烧法确定有机物的组成,为高频考点,主要考查学生运用所学化学知识综合分析和解决实际问题的能力,关键在于清楚实验的原理,掌握实验方法,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 通入CH4的电极为正极 | |
| B. | 正极的电极反应式为O2+4H++4e-═2H2O | |
| C. | 通入CH4的一极的电极反应式为CH4+2O2+4e-═CO2+2H2O | |
| D. | 负极的电极反应式为CH4+10OH--8e-═CO32-+7H2O |
| 化学式 | 电离常数 |
| CH3COOH | Ka=1.76×10-5 |
| H2SO3 | Ka1=1.54×10-2 |
| Ka2=1.02×10-7 | |
| HF | Ka=6.03×10-4 |
| A. | 在1mol•L-1NaHA(酸式盐)溶液中一定存在:c(Na+)=c(H2A)+c(HA-)+c(A2-) | |
| B. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| C. | 已知某温度下常见弱酸的电离平衡常数如上表:相同物质的量浓度的CH3COONa、NaF、Na2SO3、NaHSO3水溶液,溶液中离子总数由小到大排列的顺序是Na2SO3<CH3COONa<NaF<NaHSO3 | |
| D. | pH均等于3的醋酸与盐酸溶液等体积混合后,溶液的pH基本不变 |
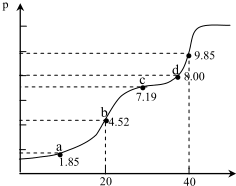
| A. | a 点所得溶液中;2n(H2A)+n(A2-)=0.002mol | |
| B. | b 点所得溶液中:c(H2A)+c(H+)=c(A2-)+c(OH-) | |
| C. | c 点所得溶液中:c(Na+)<3c(HA-) | |
| D. | d 点所得溶液中:c(Na+)>c(A2-)>c(HA-) |
| A. | 0.01 | B. | 0.10 | C. | 0.04 | D. | 0.50 |
| A. | 12.6 | B. | 13 | C. | 13.5 | D. | 13.6 |
| A. | 为提高农作物的产量和质量,应大量使用化肥和农药 | |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| C. | 实现化石燃料清洁利用,就无需开发新能源 | |
| D. | 若某个化学反应中,反应物的总能量高于生成物的总能量,则该反应为放热反应 |

 ;
; ,⑥所需的无机试剂及反应条件是氢氧化钠醇溶液、加热.
,⑥所需的无机试剂及反应条件是氢氧化钠醇溶液、加热.