题目内容
3.已知:Ka为平衡常数,pKa=-lgKa,25℃时,H2A的 pKa1=1.85,pKa2=7.19,用 0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1H2A溶液的滴定曲线如图所示(曲线上的数字为 pH).下列说法不正确的是( )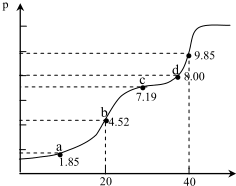
| A. | a 点所得溶液中;2n(H2A)+n(A2-)=0.002mol | |
| B. | b 点所得溶液中:c(H2A)+c(H+)=c(A2-)+c(OH-) | |
| C. | c 点所得溶液中:c(Na+)<3c(HA-) | |
| D. | d 点所得溶液中:c(Na+)>c(A2-)>c(HA-) |
分析 A.Ka1=$\frac{c(H{A}^{-}).c({H}^{+})}{c({H}_{2}A)}$,a点溶液中c(H+)=10-1.85,则该溶液中c(HA-)=$\frac{{K}_{a1}×c({H}_{2}A)}{c({H}^{+})}$=$\frac{1{0}^{-1.85}×c({H}_{2}A)}{1{0}^{-1.85}}$=c(H2A),再结合物料守恒判断;
B.20mL时,二者恰好完全反应生成NaHA,溶液中存在电荷守恒和物料守恒,根据电荷守恒和物料守恒判断;
C.c点溶液中溶质为NaHA、Na2A,溶液呈碱性,c(OH-)>c(H+),c(H+)=10-7.19mol/L,Ka2=$\frac{c({A}^{2-}).c({H}^{+})}{c(H{A}^{-})}$=10-7.19,所以c(HA-)=c(A2-),结合溶液中电荷守恒判断;
D.加入氢氧化钠溶液40ml,NaOH溶液滴定20mL0.1mol•L-1HA溶液恰好反应生成Na2A,d点溶液中主要是Na2A和少量NaHA.
解答 解:A.Ka1=$\frac{c(H{A}^{-}).c({H}^{+})}{c({H}_{2}A)}$,a点溶液中c(H+)=10-1.85,则该溶液中c(HA-)=$\frac{{K}_{a1}×c({H}_{2}A)}{c({H}^{+})}$=$\frac{1{0}^{-1.85}×c({H}_{2}A)}{1{0}^{-1.85}}$=c(H2A),再结合物料守恒知,溶液中存在n(H2A)+n(HA-)+n(A2-)=2n(H2A)+n(A2-)=0.1mol/L×0.02L=0.002mol,故A正确;
B.20mL时,二者恰好完全反应生成NaHA,溶液中存在电荷守恒和物料守恒,根据电荷守恒电荷守恒c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-),物料守恒c(Na+)=c(HA-)+c(A2-)+c(H2A),得到:c(H2A)+c(H+)=c(A2-)+c(OH-),故B正确;
C.c点溶液中溶质为NaHA、Na2A,溶液呈碱性,c(OH-)>c(H+),c(H+)=10-7.19mol/L,Ka2=$\frac{c({A}^{2-}).c({H}^{+})}{c(H{A}^{-})}$=10-7.19,所以c(HA-)=c(A2-),溶液中电荷守恒为:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-),已知(HA-)=c(A2-),则c(Na+)+c(H+)=3c(HA-)+c(OH-),由于c(OH-)>c(H+),所以c(Na+)>3c(HA-),故C错误;
D.加入氢氧化钠溶液40ml,NaOH溶液滴定20mL0.1mol•L-1H2A溶液恰好反应生成Na2A,d点溶液中主要是Na2A和少量NaHA,溶液中离子浓度c(Na+)>c(A2-)>c(HA-),故D正确;
故选C.
点评 本题考查酸碱混合溶液定性判断,为高频考点,侧重考查学生分析判断及计算能力,明确电离平衡常数概念及表达式、溶液中各点溶质成分及其性质是解本题关键,难点是电离平衡常数的灵活运用,题目难度中等.

 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案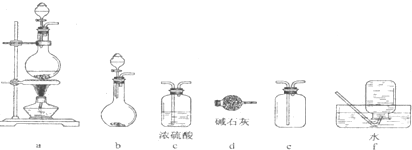
| A. | 加热浓硫酸和乙醇的混合物至170℃制备收集C2H4:连接a→d→f | |
| B. | 制备收集NO2:连接a→c→f | |
| C. | 制备收集Cl2:连接a→d→e | |
| D. | 制备收集NH3:连接b→d→e |
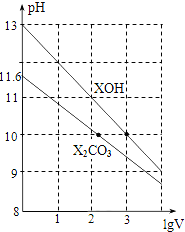
| A. | XOH是弱碱 | |
| B. | pH=10的两种溶液中的c(X+):XOH大于X2CO3 | |
| C. | 已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1.0×10-10.2 | |
| D. | 当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$减小 |
| A. | 常温下,单质铍能与水反应放出H2 | |
| B. | Be(OH)2易溶于水 | |
| C. | Be(OH)2溶于盐酸,也可能溶于NaOH溶液 | |
| D. | BeCl2中各原子中的最外层电子层都满足8电子结构 |
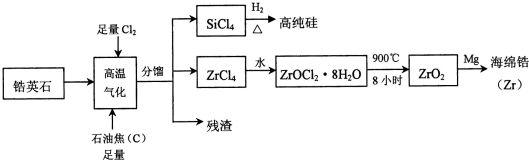
 .
.