题目内容
在特制的密闭真空容器中加入一定量纯净的氨基甲酸铵固体(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)═2NH3(g)+CO2(g),已知15℃时,平衡气体总浓度为2.4×10-3mol/L,下列说法中正确的是( )
| A、密闭容器中气体的平均相对分子质量不变则该反应达到平衡状态 |
| B、15℃时氨基甲酸铵的分解平衡常数为2.048×10-9(mol/L)3 |
| C、恒温下压缩体积,NH3的体积分数减小 |
| D、再加入一定量氨基甲酸铵,可加快反应速率 |
考点:化学平衡建立的过程,化学反应速率的影响因素,化学平衡的调控作用
专题:化学平衡专题
分析:A、反应NH2COONH4(s)═2NH3(g)+CO2(g),生成的气体的物质的量之比始终是2:1,所以气体的平均相对分子质量始终不变,故不能作为平衡状态的判断依据;
B、反应中生成的氨气和二氧化碳的浓度之比为2:1,总浓度为2.4×10-3mol/L,所以氨气的浓度为1.6×10-3mol/L,二氧化碳的浓度为8.0×10-4mol/L,所以平衡常数K=(1.6×10-3)2×8.0×10-4(mol/L)3=2.048×10-9(mol/L)3;
C、恒温下压缩体积,平衡逆向移动,但体系中两种气体的物质的量之比始终不变,所以氨气的体积分数不变;
D、固体物质的多少对化学反应速率 没有影响.
B、反应中生成的氨气和二氧化碳的浓度之比为2:1,总浓度为2.4×10-3mol/L,所以氨气的浓度为1.6×10-3mol/L,二氧化碳的浓度为8.0×10-4mol/L,所以平衡常数K=(1.6×10-3)2×8.0×10-4(mol/L)3=2.048×10-9(mol/L)3;
C、恒温下压缩体积,平衡逆向移动,但体系中两种气体的物质的量之比始终不变,所以氨气的体积分数不变;
D、固体物质的多少对化学反应速率 没有影响.
解答:
解:A、反应NH2COONH4(s)═2NH3(g)+CO2(g),生成的气体的物质的量之比始终是2:1,所以气体的平均相对分子质量始终不变,故不能作为平衡状态的判断依据,故A错误;
B、反应中生成的氨气和二氧化碳的浓度之比为2:1,总浓度为2.4×10-3mol/L,所以氨气的浓度为1.6×10-3mol/L,二氧化碳的浓度为8.0×10-4mol/L,所以平衡常数K=(1.6×10-3)2×8.0×10-4(mol/L)3=2.048×10-9(mol/L)3,故B正确;
C、恒温下压缩体积,平衡逆向移动,但体系中两种气体的物质的量之比始终不变,所以氨气的体积分数不变,故C错误;
D、固体物质的多少对化学反应速率没有影响,故D错误;
故选B.
B、反应中生成的氨气和二氧化碳的浓度之比为2:1,总浓度为2.4×10-3mol/L,所以氨气的浓度为1.6×10-3mol/L,二氧化碳的浓度为8.0×10-4mol/L,所以平衡常数K=(1.6×10-3)2×8.0×10-4(mol/L)3=2.048×10-9(mol/L)3,故B正确;
C、恒温下压缩体积,平衡逆向移动,但体系中两种气体的物质的量之比始终不变,所以氨气的体积分数不变,故C错误;
D、固体物质的多少对化学反应速率没有影响,故D错误;
故选B.
点评:本题主要考查了平衡状态的判断、平衡常数的计算、平衡移动的影响因素,难度中等,解题时要注意氨基甲酸铵是固体.

练习册系列答案
相关题目
下列叙述错误的是( )
| A、漂白粉要密闭保存 |
| B、等量的铝分别与足量的盐酸和氢氧化钠溶液反应产生氢气的量相同 |
| C、常温下铁和浓硫酸能发生化学反应 |
| D、工业上用电解氯化铝的方法来制取金属铝 |
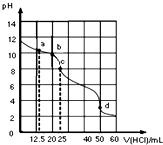 在常温下,0.1000mol?L-1Na2CO3溶液25mL 用0.1000mol?L-1盐酸滴定,其滴定曲线如图.对滴定过程中所得溶液中相关离子浓度间的关系,下列有关说法正确的是( )
在常温下,0.1000mol?L-1Na2CO3溶液25mL 用0.1000mol?L-1盐酸滴定,其滴定曲线如图.对滴定过程中所得溶液中相关离子浓度间的关系,下列有关说法正确的是( )| A、a点:c(CO32-)=c(HCO3-)>c(OH-) |
| B、b点:5c(Cl-)=4c(HCO3-a点:c(CO32-)=c(HCO3-)>c(OH-))+4c(CO32-) |
| C、c点:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
| D、d点:c(Na+)<c(Cl-)+ |
下列图示与对应的叙述相符的是( )
A、 说明烯烃与H2的加成反应是放热反应,虚线表示在有催化剂的条件下进行 |
B、 用0.1000mol/LNaOH溶液分别滴定浓度相同的三种一元酸,由图曲线可确定①的酸性最强 |
C、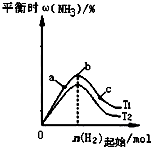 图表示合成氨反应在其他条件不变的情况下,改变n(H2)起始对平衡的影响.由此可知,N2的转化率最高的是b点;且T1>T2,K2>K1(T1和T2表示温度,K1、K2表示对应温度下的平衡常数) |
D、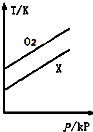 在体积相同的两个密闭容器中,分别充入等质量的O2和X气体,由图可确定X可能是CH4 |
下列有关物质用途的叙述中,错误的是( )
| A、可用明矾或硫酸铁对水净化 |
| B、可利用2Fe3++Cu═Cu2++2Fe2+腐蚀印刷电路板 |
| C、自然界中硅以单质形式大量存在,所以才可以广泛应用于电子工业中 |
| D、水玻璃是制备硅胶和木材防火剂的原料 |
对于反应8LiCoO2+Na2S2O3+□ =4Li2SO4+8CoSO4+Na2SO4+□ ,下列说法正确的是( )
| A、Na2S2O3在反应中被还原为Na2SO4 |
| B、0.1mol Na2S2O3在反应中转移0.4mol电子 |
| C、反应中的未知物的系数均为11 |
| D、还原性LiCoO2大于CoSO4 |
下列实验操作正确的是( )
| A、中和滴定实验时,用待测液润洗锥形瓶 |
| B、盛放Na2CO3溶液时,使用带玻璃塞的磨口瓶 |
| C、将三氯化铝溶液蒸干,可制得三氯化铝固体 |
| D、锌与稀硫酸反应时,要加大反应速率可滴加少量硫酸铜 |
下列各组离子在指定溶液中能大量共存的是( )
| A、无色溶液中:K+、Na+、MnO4-、SO42- |
| B、酸性溶液中:Cl-、Na+、AlO2-、NO3- |
| C、加入Al能放出H2的溶液中:Cl-、HCO3-、SO42-、NH4+ |
| D、有较多Fe3+的溶液中:Na+、NH4+、Cl-、SO42- |
下列的叙述中,正确的是( )
| A、检验溴乙烷中的溴元素,加入NaOH溶液共热,冷却后加入AgNO3溶液,观察有无浅黄色沉淀生成 |
| B、苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO2-3 |
| C、苯酚能与FeCl3溶液反应生成紫色沉淀 |
| D、苯酚有强腐蚀性,沾在皮肤上可用酒精清洗 |