题目内容
15.在恒温时,一固定容积的容器内发生如下反应:N2O4(g)?2NO2(g)达到平衡时,再向容器内通入一定量的N2O4(g),重新达到平衡后,与第一次平衡时相比,N2O4的体积分数( )| A. | 不变 | B. | 增大 | C. | 减小 | D. | 无法判断 |
分析 恒温恒容条件下下,到达平衡时再向容器内通入一定量的N2O4(g),等效为在原平衡基础上增大压强,平衡向着气体体积缩小的方向移动,据此进行解答.
解答 解:恒温恒容下,N2O4(g)?2NO2(g)达到平衡时再向容器内通入一定量的N2O4(g),等效为在原平衡基础上增大压强,平衡向着逆向移动,N2O4(g)的体积分数增大,NO2的体积分数减小,
故选B.
点评 本题考查化学平衡影响因素,题目难度不大,明确化学平衡及其影响为解答关键,注意理解利用等效思想构建平衡建立的途径,试题培养了学生的灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
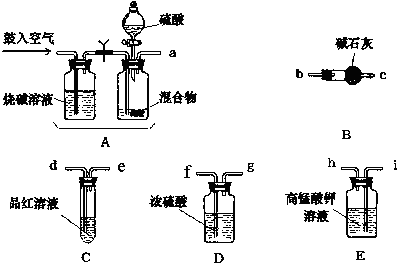
6.根据测定硫酸铜晶体中结晶水含量的实验,填写下列空白:
(1)本实验至少需要加热2次.至少需要称量4次.
(2)通过实验知道,要确保结果的准确性,本实验中的一个关键是通过恒重操作来判断硫酸铜晶体加热时是否完全变成无水硫酸铜.
(3)学生甲实验得到以下的数据:
甲学生结晶水数量的测定值5.23(保留2位小数)
(4)若学生乙的实验结果偏低,从下列选项中选出造成结果偏低的可能原因de(填序号).
a.加热前称量时坩埚未完全干燥 b.加热过程中有少量晶体溅出
c.加热时坩埚内物质变黑 d.加热后放在空气中冷却
e.最后两次加热后称量的质量差大于0.001g.
(1)本实验至少需要加热2次.至少需要称量4次.
(2)通过实验知道,要确保结果的准确性,本实验中的一个关键是通过恒重操作来判断硫酸铜晶体加热时是否完全变成无水硫酸铜.
(3)学生甲实验得到以下的数据:
| 坩埚质量(g) | 坩埚和晶体的总质量(g) | 加热后坩埚和剩余固体的质量(g) |
| 11.685 | 13.691 | 12.948 |
(4)若学生乙的实验结果偏低,从下列选项中选出造成结果偏低的可能原因de(填序号).
a.加热前称量时坩埚未完全干燥 b.加热过程中有少量晶体溅出
c.加热时坩埚内物质变黑 d.加热后放在空气中冷却
e.最后两次加热后称量的质量差大于0.001g.
3.(1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.单位质量的A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
①某同学根据上述信息,推断B的核外电子排布如图1所示,该同学所画的电子排布图违背能量最低原理,B元素位于周期表五个区域中的s区.

②ACl2分子中A的杂化类型为sp杂化,ACl2的空间构型为直线形.
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物.
①以体心立方堆积形成的金属铁中,其原子的配位数为8.
②写出一种与CN-互为等电子体的单质的电子式 .
.
③六氰合亚铁离子[Fe(CN)6]4-中不存在B.
A.共价键 B.非极性键 C.配位键 D.σ键 E.π键
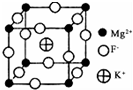
(3)一种Al-Fe合金的立体晶胞如图2所示.请据此回答下列问题:
①确定该合金的化学式Fe2Al.
②若晶体的密度=ρ g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为$\root{3}{\frac{139}{2ρ{N}_{A}}}$cm.
| 电离能(KJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15399 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |

②ACl2分子中A的杂化类型为sp杂化,ACl2的空间构型为直线形.
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物.
①以体心立方堆积形成的金属铁中,其原子的配位数为8.
②写出一种与CN-互为等电子体的单质的电子式
 .
.③六氰合亚铁离子[Fe(CN)6]4-中不存在B.
A.共价键 B.非极性键 C.配位键 D.σ键 E.π键
(3)一种Al-Fe合金的立体晶胞如图2所示.请据此回答下列问题:
①确定该合金的化学式Fe2Al.
②若晶体的密度=ρ g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为$\root{3}{\frac{139}{2ρ{N}_{A}}}$cm.
20.下列元素的电负性最大的是( )
| A. | O | B. | S | C. | P | D. | C |
5.下列说法正确的是( )
| A. | 置换反应不一定全部是氧化还原反应 | |
| B. | 氧化还原反应中氧化剂和还原剂可以是同种物质 | |
| C. | 氧化反应和还原反应不一定同时发生 | |
| D. | 还原剂是得电子,氧化剂失电子 |
 卤族元素是典型的非金属元素,单质及其化合物在工农业生产和生活中有重要的用途.
卤族元素是典型的非金属元素,单质及其化合物在工农业生产和生活中有重要的用途. 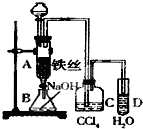 某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.
某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.