题目内容
5.把0.5mol X气体和0.5mol Y气体混合于2L密闭容器中,使它们发生如下反应:2X(g)+Y(g)?nM(g)+2W(g).2min末,容器内气体的总物质的量与反应前容器内气体的总物质的量之比为6:5,若测知以W的浓度变化表示的反应速率为0.05mol•L-1•min-1,计算:(1)前2min内用Y的浓度变化表示的平均反应速率为0.025mol•L-1•min-1.
(2)2min末X的转化率为40%.
(3)反应化学方程式中n=3.
分析 测知以W的浓度变化表示的反应速率为0.05mol•L-1•min-1,则生成W为0.05mol•L-1•min-1×2min×2L=0.2mol,则
2X(g)+Y(g)?nM(g)+2W(g)
开始 0.5 0.5 0 0
转化 0.2 0.1 0.1n 0.2
2min 0.3 0.4 0.1n 0.2
容器内气体的总物质的量与反应前容器内气体的总物质的量之比为6:5,
则$\frac{0.3+0.4+0.1n+0.2}{0.5+0.5}$=$\frac{6}{5}$,
解得n=3,以此来解答.
解答 解:测知以W的浓度变化表示的反应速率为0.05mol•L-1•min-1,则生成W为0.05mol•L-1•min-1×2min×2L=0.2mol,则
2X(g)+Y(g)?nM(g)+2W(g)
开始 0.5 0.5 0 0
转化 0.2 0.1 0.1n 0.2
2min 0.3 0.4 0.1n 0.2
容器内气体的总物质的量与反应前容器内气体的总物质的量之比为6:5,
则$\frac{0.3+0.4+0.1n+0.2}{0.5+0.5}$=$\frac{6}{5}$,
解得n=3,
(1)速率之比等于化学计量数之比,则前2min内用Y的浓度变化表示的平均反应速率为0.05mol•L-1•min-1×$\frac{1}{2}$=0.025mol•L-1•min-1,
故答案为:0.025mol•L-1•min-1;
(2)2min末X的转化率为$\frac{0.2}{0.5}$×100%=40%,
故答案为:40%;
(3)由上述计算可知,反应化学方程式中n=3,故答案为:3.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、反应速率及转化率的计算为解答的关键,侧重分析与计算能力的考查,注意物质的量比等于压强比,题目难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 主族元素的电负性越大,元素原子的第一电离能一定越大 | |
| B. | 在元素周期表中,元素电负性从左到右越来越小 | |
| C. | 在形成化合物时,电负性越小的元素越容易显正价 | |
| D. | 金属元素的电负性一定小于非金属元素的电负性 |
| A. | 同族元素,随着核外电子层数的增加,I1逐渐增大 | |
| B. | 通常情况下,对于同一种元素的原子,其电离能I1<I2<I3 | |
| C. | 同周期元素,总体变化趋势是随着核电荷数的增加,I1增大 | |
| D. | 通常情况下,电离能越小,元素的金属性越强 |

 ①盐泥a除泥沙外,还含有的物质是Mg(OH)2.
①盐泥a除泥沙外,还含有的物质是Mg(OH)2.
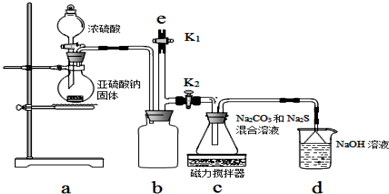
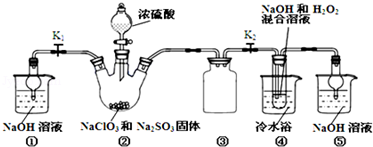
 某课外活动小组探索苯与液溴的反应是否属于取代反应,设计了如下实验装置.
某课外活动小组探索苯与液溴的反应是否属于取代反应,设计了如下实验装置.