题目内容
7.将固体NH4I置于密闭容器中,在一定温度下发生下列反应①NH4I(s)?NH3(g)+HI(g);②2HI(g)?H2(g)+I2(g).达到平衡时,c(H2)=1mol/L,c(HI)=3mol/L,则此温度下反应①的平衡常数为( )| A. | 3 | B. | 9 | C. | 12 | D. | 15 |
分析 反应①的平衡常数k=c(NH3)•c(HI),NH4I分解生成的HI为平衡时HI与分解的HI之和,即为NH4I分解生成的NH3,由反应②可知分解的c(HI)为平衡时c(H2)的2倍,求出为NH4I分解生成的NH3,代入反应①的平衡常数K=c(NH3)•c(HI)计算.
解答 解:平衡时c(HI)=4mol•L-1,HI分解生成的H2的浓度为1mol•L-1,则:
NH4I分解生成的HI的浓度为3mol•L-1+2×1mol•L-1=5mol•L-1,
所以NH4I分解生成的NH3的浓度为5mol•L-1,
所以反应①的平衡常数k=c(NH3)•c(HI)=5mol•L-1×3mol•L-1=15mol2•L-2.
故选:D.
点评 本题考查化学平衡常数的计算,解题关键在于平衡时HI为NH4I分解生成的HI与分解的HI之差,难度中等.

练习册系列答案
相关题目
17.下列说法正确的是( )
| A. | 在相同温度下,饱和溶液一定比不饱和溶液导电性强 | |
| B. | 氯化钠溶液在电流作用下电离成钠离子和氯离子 | |
| C. | 晶体NaCl不导电,所以它不是电解质,而铜、铁等金属能导电,所以它们是电解质 | |
| D. | 氯化氢溶于水能导电,但液态氯化氢不导电 |
18.在盛有饱和Na2CO3溶液的烧杯中,插入两个Pt电极,保持温度不变,通电一段时间后,下列判断正确的是( )
| A. | 溶液的pH将增大 | B. | Na+数和CO32-数的比值将变小 | ||
| C. | 溶液浓度不变,有晶体析出 | D. | 溶液浓度逐渐增大并有晶体析出 |
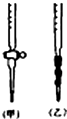
15.某同学做如表实验:下列说法正确的是( )
| 装 置 | 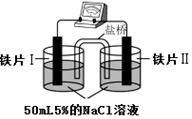 | 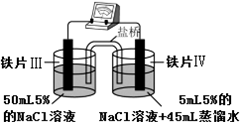 |
| 现象 | 电流计指针未发生偏转 | 电流计指针发生偏转 |
| A. | “电流计指针未发生偏转”,说明铁片Ⅰ、铁片Ⅱ均未被腐蚀 | |
| B. | 铁片Ⅳ的电极反应式可能为Fe-3e-=Fe3+ | |
| C. | 用K3Fe(CN)6]溶液检验铁片Ⅲ、Ⅳ附近溶液,可判断装置的正、负极 | |
| D. | 铁片Ⅰ、Ⅲ所处的电解质溶液浓度相同,所以二者的腐蚀速率相等 |
2.如图是金属牺牲阳极的阴极保护法的实验装置,有关说法正确的是( )
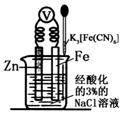

| A. | 该装置为电解池 | |
| B. | 本实验牺牲了金属Fe来保护金属Zn | |
| C. | 若加入K3[Fe(CN)6]溶液后,Fe电极附近不会产生特征蓝色的沉淀 | |
| D. | 远洋货轮上镶嵌的金属Zn长时间没有什么变化,不需要更换 |
12.下列物质属于硅酸盐的是( )
| A. | 二氧化硅 | B. | 保鲜膜 | C. | 青花瓷 | D. | 金刚石 |
19.化学源于生活,同时又服务于生活.以下做法不合理的是( )
| A. | 用食醋除去暖水瓶中的薄层水垢 | |
| B. | 一般不用纯碱代替小苏打作食品发酵粉 | |
| C. | 用甲醛溶液浸泡海产品以保鲜 | |
| D. | 用灼烧并闻气味的方法区别纯棉织物和纯毛织物 |
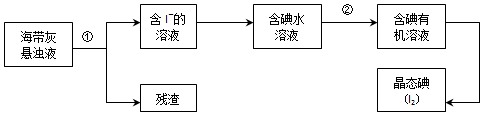
 阅读下列实验内容,根据题目要求回答问题:
阅读下列实验内容,根据题目要求回答问题: