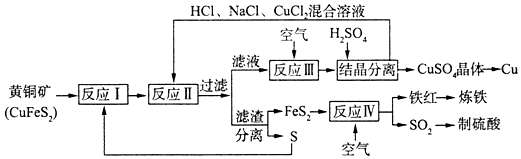
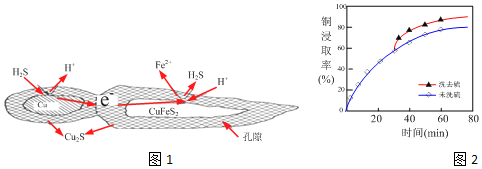
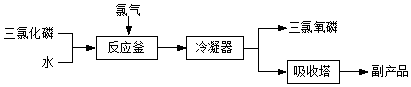
题目内容
9.已知某反应aA(g)+bB(g)?cC(g)的各物质浓度数据如表:| A | B | C | |
| 起始浓度(mol/L) | 3.0 | 2.0 | 0 |
| 2s末浓度(mol/L) | 0.6 | 0.4 | 0.8 |
| A. | 3:1:2 | B. | 3:2:1 | C. | 2:1:3 | D. | 9:3:4 |
分析 由表格中数据可知,
aA(g)+bB(g)?cC(g)
开始 3.0 2.0 0
转化 2.4 1.6 0.8
6s 0.6 0.4 0.8
结合转化的量等于速率之比,也等于化学计量数之比计算.
解答 解:由表格中数据可知,
aA(g)+bB(g)?cC(g)
开始 3.0 2.0 0
转化 2.4 1.6 0.8
6s 0.6 0.4 0.8
则上述方程式中各物质的化学计量数之比是2.4mol/L:1.6mol/L:0.8mol/L=3:2:1,
故选B.
点评 本题考查化学平衡的计算,为高频考点,把握表格中数据、浓度变化与化学计量数的关系为解答的关键,侧重分析与计算能力的考查,注意数据分析与应用,题目难度不大.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
19.已知H2A为二元弱酸,室温时,配制一组c(H2A)+c(HA-)+c(A2-)=0.100mol•L-1的H2A和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示,下列指定溶液中微粒的物质的量浓度关系不正确的是( )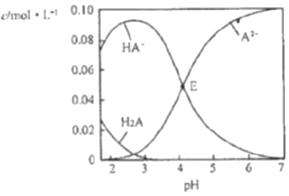

| A. | pH=2的溶液中:c(H2A)+c(A2-)>c(HA-) | |
| B. | E点溶液中:c(Na+)-c(HA-)<0.100mol•L-1 | |
| C. | c(Na+)=0.100mol•L-1的溶液中:c(H+)+c(H2A)=c(OH-)+c(A2-) | |
| D. | pH=7的溶液中:c(Na+)>2c(A2-) |
20.氯苯在染料、医药工业中有广泛的应用,某实验小组利用如图装置合成氯苯(支撑用的铁架台部分省略)并通过一定操作提纯氯苯.
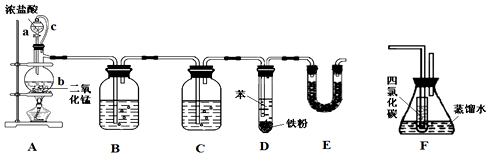
反应物和产物的相关数据列表如下:
请按要求回答下列问题.
(1)装置A中橡胶管c的作用是,装置E的作用是除去氯气和氯化氢气体,防止大气污染.
(2)实验时;使a中的浓盐酸缓缓滴下,可观察到仪器b内的现象是有黄绿色气体生成,写出反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(3)为证明氯气和苯发生的是取代而不是加成反应,该小组用装置F说明,则装置F置于D和E之间(填字母),F中小试管内CCl4的作用是除去氯气,还需使用的试剂是硝酸酸化的硝酸银溶液.
(4)已知D中加入5mL苯,经过提纯后收集到氯苯3.0g,则氯苯的产率为47.3%(保留三位有效数字).

反应物和产物的相关数据列表如下:
| 密度/g•cm-3 | 沸点/℃ | 水中溶解性 | |
| 苯 | 0.879 | 80.1 | 微溶 |
| 氯苯 | 1.11 | 131.7 | 不溶 |
(1)装置A中橡胶管c的作用是,装置E的作用是除去氯气和氯化氢气体,防止大气污染.
(2)实验时;使a中的浓盐酸缓缓滴下,可观察到仪器b内的现象是有黄绿色气体生成,写出反应的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(3)为证明氯气和苯发生的是取代而不是加成反应,该小组用装置F说明,则装置F置于D和E之间(填字母),F中小试管内CCl4的作用是除去氯气,还需使用的试剂是硝酸酸化的硝酸银溶液.
(4)已知D中加入5mL苯,经过提纯后收集到氯苯3.0g,则氯苯的产率为47.3%(保留三位有效数字).
17.下列不能用于鉴别SO2和CH4两种无色气体的试剂是( )
| A. | 氢氧化钠溶液 | B. | 品红溶液 | ||
| C. | 澄清石灰水 | D. | 酸性高锰酸钾溶液 |
4.下列反应表示氮的固定作用的是( )
| A. | N2与H2在一定条件下合成NH3 | B. | NH3经催化氧化生成NO | ||
| C. | NO和O2反应生成NO2 | D. | 由NH3制碳铵和尿素 |
1.NA表示阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 常温常压下,74g乙酸甲酯中含共用电子对数为11NA | |
| B. | 1mol Cl2通入足量的水中,转移电子数为NA | |
| C. | 足量的铁粉与200mL1 mol•L-1硝酸完全反应生成H2的分子败为0.1NA | |
| D. | 30g葡萄糖和乙酸的混合物中含碳原子数为2NA |
18.已知X、Y元素同周期,且电负性X大于Y,下列说法一定错误的是( )
| A. | 第一电离能:Y小于X | |
| B. | 气态氢化物的稳定性:Y大于X | |
| C. | 最高价含氧酸的酸性:X强于Y | |
| D. | X和Y形成化合物时,X显负价,Y显正价 |