题目内容
4.下列反应表示氮的固定作用的是( )| A. | N2与H2在一定条件下合成NH3 | B. | NH3经催化氧化生成NO | ||
| C. | NO和O2反应生成NO2 | D. | 由NH3制碳铵和尿素 |
分析 将空气中游离态的氮转化为含氮化合物的过程叫氮的固定,据此解答.
解答 解:A.N2与H2在一定条件下合成NH3,空气中游离态的氮转化为含氮化合物,属于氮的固定,故A正确;
B.NH3经催化氧化生成NO,是氮的一种化合物转化为另一种化合物,不属于氮的固定,故B错误;
C.NO和O2反应生成NO2,是氮的一种化合物转化为另一种化合物,不属于氮的固定,故C错误;
D.由NH3制碳铵和尿素,是氮的一种化合物转化为另一种化合物,不属于氮的固定,故D错误;
故选:A.
点评 本题主要考查氮的固定,题目难度不大,明确氮的固定的概念为解答关键,注意掌握氮的固定的类型及判断方法,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
相关题目
14.镭元素位于元素周期表第七周期ⅡA族.下列关于镭的性质的说法不正确的是( )
| A. | 氢氧化物呈两性 | B. | 单质与水反应放出氢气 | ||
| C. | 在化合物中呈+2价 | D. | 单质的还原性比镁强 |
15.既能和盐酸反应,又能和氢氧化钠溶液反应的物质是( )
| A. | Fe | B. | Fe2O3 | C. | Al | D. | AlCl3 |
12.NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如左图;研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如右图.下列说法正确的是( )


| A. | NH3催化还原NO为吸热反应 | |
| B. | 过程Ⅰ中NH3断裂非极性键 | |
| C. | 过程Ⅱ中NO为氧化剂,Fe2+为还原剂 | |
| D. | 脱硝的总反应为:4NH3(g)+4NO(g)+O2(g) $\stackrel{催化剂}{?}$4N2(g)+6H2O(g) |
9.已知某反应aA(g)+bB(g)?cC(g)的各物质浓度数据如表:
据此可推算出上述方程式中各物质的化学计量数之比是( )
| A | B | C | |
| 起始浓度(mol/L) | 3.0 | 2.0 | 0 |
| 2s末浓度(mol/L) | 0.6 | 0.4 | 0.8 |
| A. | 3:1:2 | B. | 3:2:1 | C. | 2:1:3 | D. | 9:3:4 |
16.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 若将lmol氯化铁完全转化为氢氧化铁胶体,则分散系中胶体微粒数为NA | |
| B. | lmolCH3COONa和少量CH3COOH溶于水所得中性溶液中,CH3COO-的数目为NA | |
| C. | 标准状态下,2.24LC12溶于水,转移的电子数目为0.1NA | |
| D. | 标准状况下,11.2L三氯甲烷所含的原子数为2NA |
13.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中A、B同主族,B、C、D、E同周期,B的核外电子数为C的$\frac{1}{2}$,D的最外层电子数为C、E之和的一半. 下列说法正确的是( )
| A. | A、B能形成离子化合物,且A离子半径小于B离子半径 | |
| B. | A、D能形成离子化合物DA5,与水反应可产生两种气体 | |
| C. | C、D的简单氢化物中只有D溶于水,其水溶液呈酸性 | |
| D. | E形成的两种氢化物中所有化学键种类完全相同 |
14.下列说法正确的是( )
| A. | 向 NaAlO2溶液中滴加 NaHCO3 溶液,有沉淀和气体生成 | |
| B. | Na、Mg、Fe 等金属在一定条件下与水反应都生成 H2和对应的碱 | |
| C. | 同主族元素的简单阴离子还原性越强,水解程度越大 | |
| D. | 符合通式 CnH2n+2的不同烃不一定互为同系物 |
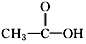 和
和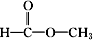 两种.为对其结构进行鉴定,物理方法可用红外光谱法或核磁共振氢谱法.
两种.为对其结构进行鉴定,物理方法可用红外光谱法或核磁共振氢谱法.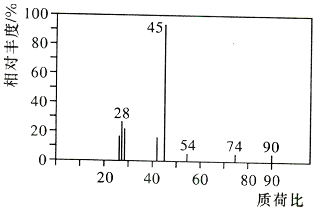
 .
.