题目内容
20.为什么都含有Na+、Cl-的NaCl晶体和NaCl溶液一个导电,另一个不导电?分析 根据含有自由移动的离子或者电子能导电分析判断.
解答 解:因为含有自由移动的离子或者电子才能导电,则NaCl晶体虽含Na+、Cl-,但不能自由移动而不能导电.NaCl溶液中离子可以自由移动,可以导电,故答案为:NaCl晶体虽含Na+、Cl-,但不能自由移动而不能导电.NaCl溶液中离子可以自由移动,可以导电.
点评 本题考查了物质导电的原理,难度不大,注意基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.25℃时,下列关系式正确的是( )
| A. | pH=2的CH3COOH 溶液与pH=12的NaOH溶液等体积混合:c(Na+)=c(CH3COO-)>c(CH3COOH) | |
| B. | pH=3的H2C2O4溶液:c(H+)═c(HC2O4-)+c(OH-)=1×10-3mol/L | |
| C. | pH相同的①NH4HSO4、②NH4Cl、③(NH4)2SO4三种溶液的c(NH4+):③>①>② | |
| D. | 盐酸与FeCl3的混合溶液pH=2,稀释10倍后:pH<3 |
8.加热N2O5,依次发生分解反应:①N2O5(g)?N2O3(g)+O2(g)、②N2O3(g)?N2O(g)+O2(g).在体积为2L的恒容密闭容器中充入8mol N2O5,加热到T℃时O2和N2O3的物质的量分别为9mol、3.4mol,则T℃时$\frac{c({N}_{2}{O}_{3})•c({O}_{2})}{c({N}_{2}{O}_{5})}$为( )
| A. | 10.7 | B. | 8.5 | C. | 9.6 | D. | 10.2 |
15.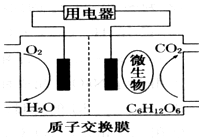 微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( )
微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( )
 微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( )
微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( )| A. | 正极反应中有CO2生成 | |
| B. | O2在正极反应 | |
| C. | H+通过交换膜从负极区移向正极区 | |
| D. | 电池总反应为C6H12O6+6O2═6CO2+6H2O |
5.将m g含Fe2O3•nH2O的Al2O3溶于200mL 0.05mol/L的硫酸溶液中,然后加入100mLNH3•H2O,使溶液的Fe3+和Al3+恰好完全沉淀,则NH3•H2O的浓度为( )
| A. | 0.2mol/L | B. | 0.1mol/L | C. | 0.05mol/L | D. | 0.02 mol/L |
9.下列仪器能直接用酒精灯加热的是( )
①量筒 ②表面皿 ③烧杯 ④试管⑤容量瓶 ⑥蒸发皿 ⑦坩埚 ⑧烧瓶.
①量筒 ②表面皿 ③烧杯 ④试管⑤容量瓶 ⑥蒸发皿 ⑦坩埚 ⑧烧瓶.
| A. | ②③④⑥⑦⑧ | B. | ③⑥⑧ | C. | ④⑥⑦ | D. | ④⑦⑧ |
10. 已知t℃时AgCl的Ksp=2×10-10,Ag2CrO4(橙红色固体)在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
已知t℃时AgCl的Ksp=2×10-10,Ag2CrO4(橙红色固体)在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
 已知t℃时AgCl的Ksp=2×10-10,Ag2CrO4(橙红色固体)在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
已知t℃时AgCl的Ksp=2×10-10,Ag2CrO4(橙红色固体)在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )| A. | 在t℃时,Ag2CrO4的Ksp为1×10-9 | |
| B. | 在饱和Ag2CrO4溶液中加入K2CrO4可使溶液由Y 点到X点 | |
| C. | 在t℃时,AgCl的溶解度大于Ag2CrO4 | |
| D. | 在t℃时,以0.01 mol/L AgNO3溶液滴定20mL未 知浓度的KCl溶液,可用K2CrO4做指示剂 |