题目内容
10.化学与人类社会的生产、生活有着密切联系.下列叙述中正确的是( )| A. | 火箭用偏二甲肼(C2H8N2)作燃料,N2O4作还原剂,反应产生巨大能量 | |
| B. | 铝制品由于表面有致密的氧化膜,可以稳定存在于空气中 | |
| C. | 硫是一种生命元素,自然界中的石膏矿、硫铁矿、赤铁矿等都是含“硫”为主的矿石 | |
| D. | 高纯度的SiO2对光有很好的折射和全反射作用,可以制成光电池将光能直接转化为电能 |
分析 A.发生C2H8N2+2N2O4$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O+3N2,N2O4中N元素的化合价降低;
B.Al表面的氧化膜为致密结构;
C.赤铁矿的主要成分氧化铁;
D.SiO2为光导纤维的材料.
解答 解:A.火箭用偏二甲肼(C2H8N2)作燃料,N2O4作氧化剂,为放热的氧化还原反应,反应产生巨大能量,故A错误;
B.Al表面的氧化膜为致密结构,可以稳定存在于空气中,故B正确;
C.赤铁矿的主要成分氧化铁,而自然界中的石膏矿、硫铁矿等都是含“硫”为主的矿石,故C错误;
D.SiO2为光导纤维的材料,利用Si制成的太阳能板将光能直接转化为电能,故D错误;
故选B.
点评 本题考查物质的性质、应用等,为高频考点,把握物质的性质、发生的反应等为解答的关键,侧重分析、应用能力的考查,注意化学与生活的联系及应用,题目难度不大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
17.X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的3倍.下列说法中正确的是( )

| A. | 原子半径Y>X | |
| B. | 最高价氧化物对应水化物的酸性:Z>W | |
| C. | 四种元素的单质中,Z单质的熔、沸点最高 | |
| D. | Z的单质与足量的单质Y反应,直接得到一种ZY3的物质 |
1.下列说法不正确的是( )
| A. | 室温下,NH4Cl溶液加水稀释过程中,$\frac{c(N{H}_{3}•{H}_{2}O)}{c(N{{H}_{4}}^{+})}$数值增大 | |
| B. | O.lOOOmol•L-1 的醋酸钠溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1000mol•L-1 | |
| C. | 室温下,0.1mol•L-1NaHCO3溶液的pH=8.31,则Ka1(H2CO3)×Ka2(H2CO3)<K | |
| D. | 室温,Ka(CH3COOH)=l.76×l0-5,Kb(NH3•H2O)=1.76×lO-5.则CH3COONH4溶液中存在:c(NH4+)=c(CH3COO-)>c(H+)=c(OH-)>c(NH3•H2O)=c(CH3COOH) |
5.下列说法正确的是( )
| A. | 2.0 g H218O与2H2O的混合物中所含中子数约为6.02×1023 | |
| B. | 2Mg(s)+CO2(g)=C(s)+2MgO(s)在一定条件下能自发进行,说明该反应的△H<0 | |
| C. | 向硫酸钡悬浊液中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,向沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3) | |
| D. | 向浑浊的苯酚试液中加饱和Na2CO3溶液,试液变澄清,说明苯酚的酸性强于碳酸 |
15.短周期主族元素W、X、Y、Z的原子序数依次增大.元素W的原子内层电子数是最外层电子数的2倍,元素X的单质是电池常用的惰性电极材料,元素Y的原子最外层电子数等于电子层数,元素Z的原子最外层电子数是其电子层数的2倍.下列说法错误的是( )
| A. | 化合物XZ2中,各原子均满足8电子的稳定结构 | |
| B. | 元素X与氢元素能形成原子数目之比为1:1的化合物 | |
| C. | Y的单质与稀硫酸、浓硫酸均可发生氧化还原反应 | |
| D. | Z的单质在加热条件下会与Fe反应生成Fe3Z4 |
19.X、Y、Z、W均为短周期主族元素,X与W、Y与Z分别位于同一周期,X、Y、Z的最外层电子数依次增大,W的最外层电子数是X与Y的最外层电子数之和,Z的最简单氢化物为甲,W的最简单氢化物为乙,乙是双原子分子且甲、乙混合时有白烟生成,下列说法正确的是( )
| A. | 原子半径:X>W>Z>Y | |
| B. | 化合物ZW3溶于水时水解生成一种弱碱和一种强酸 | |
| C. | X的最高价氧化物能与Z的最高价氧化物对应的水化物反应 | |
| D. | 甲、乙混合时生成的白烟为离子化合物,且该化合物只含有离子键 |
20.关于由铜、锌和稀硫酸组成的原电池中,下列各叙述正确的是( )
| A. | 负极附近c(Zn2+)减小 | |
| B. | 溶液的pH变小 | |
| C. | H+向负极移动 | |
| D. | 若Cu,Zn两极上同时有气泡逸出,则说明Zn片不纯 |
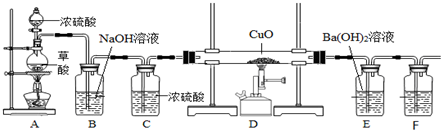
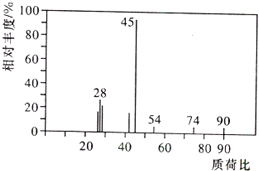 有机物A常用于食品行业.已知9.0g A在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2.
有机物A常用于食品行业.已知9.0g A在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2.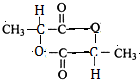 +2H2O;
+2H2O;