题目内容
20.关于由铜、锌和稀硫酸组成的原电池中,下列各叙述正确的是( )| A. | 负极附近c(Zn2+)减小 | |
| B. | 溶液的pH变小 | |
| C. | H+向负极移动 | |
| D. | 若Cu,Zn两极上同时有气泡逸出,则说明Zn片不纯 |
分析 锌、铜和稀硫酸组成的原电池中,锌作负极,负极上锌失电子发生氧化反应,电极反应:Zn-2e-═Zn2+;铜作正极,正极上氢离子得电子发生还原反应电极方程式为2H++2e-=H2↑,原电池工作时,阳离子向正极移动,阴离子向负极移动,以此解答该题.
解答 解:A.负极发生Zn-2e-═Zn2+,c(Zn2+)增大,故A错误;
B.正极发生2H++2e-=H2↑,氢离子浓度变小,则pH增大,故B错误;
C.原电池工作时,氢离子向正极移动,故C错误;
D.如为纯锌、纯铜,则只有正极上生成气体,如Cu,Zn两极上同时有气泡逸出,则说明Zn片不纯,也形成原电池反应,故D正确.
故选D.
点评 本题考查原电池知识,侧重于学生的分析能力和电化学知识的综合考查,为高考常见题型和高频考点,注意把握原电池的工作原理,难度不大.

练习册系列答案
相关题目
10.化学与人类社会的生产、生活有着密切联系.下列叙述中正确的是( )
| A. | 火箭用偏二甲肼(C2H8N2)作燃料,N2O4作还原剂,反应产生巨大能量 | |
| B. | 铝制品由于表面有致密的氧化膜,可以稳定存在于空气中 | |
| C. | 硫是一种生命元素,自然界中的石膏矿、硫铁矿、赤铁矿等都是含“硫”为主的矿石 | |
| D. | 高纯度的SiO2对光有很好的折射和全反射作用,可以制成光电池将光能直接转化为电能 |
8.为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2,CO2,SO2,NO,CO,不考虑其他成分),设计了如下流程: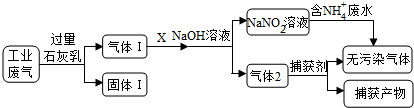
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 固体Ⅰ中主要含有Ca(OH)2、CaCO3、CaSO3 | |
| B. | X可以是空气,且需过量 | |
| C. | 捕获剂所捕获的气体主要是CO | |
| D. | 处理含NH4+废水时,发生反应的离子方程式为:NH4++NO2-=N2↑+2H2O |
5.下列离子方程式正确的是( )
| A. | 氯气与氢氧化钠溶液反应:Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | 碳酸钙加入盐酸中:CO32-+2H+═H2O+CO2↑ | |
| C. | 铁与FeCl3溶液反应:Fe+Fe3+═2Fe2+ | |
| D. | 向MgCl2溶液加入氨水:Mg2++2OH-═Mg(OH)2↓ |
12.下列说法正确的是( )
| A. | 水是无机物,故有机物在水中的溶解度都很小 | |
| B. | 氢键对物质的溶解性没有影响 | |
| C. | 溶质能与水发生化学反应将增大其在水中的溶解度 | |
| D. | CO与水都是极性分子,故CO易溶于水 |
4.四种仪器中,不能用来加热的是( )
| A. |  | B. |  | C. |  | D. |  |
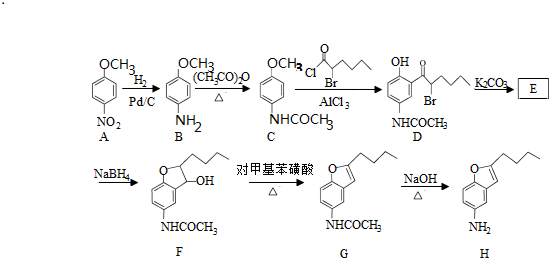
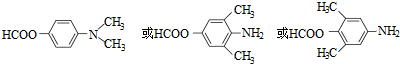 .
.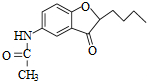 .
.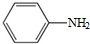 )易被氧化
)易被氧化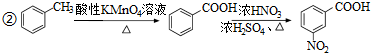
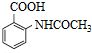 ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干). ;
; ;
;