题目内容
2.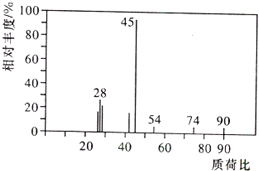 有机物A常用于食品行业.已知9.0g A在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2.
有机物A常用于食品行业.已知9.0g A在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2.(1)A分子的质谱图如图所示,从图中可知其相对分子质量是90,则A的分子式是C3H6O3;
(2)A能与NaHCO3溶液发生反应,A一定含有的官能团名称是羧基.
(3)A分子的核磁共振氢谱有4个吸收峰,峰面积之比是1:1:1:3,则A的结构简式是CH3CH(OH)COOH;
(4)写出两分子A生成六元环酯的化学方程式:2CH3CH(OH)COOH $→_{△}^{浓硫酸}$
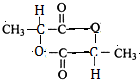 +2H2O;
+2H2O;(5)请写出官能团与A相同的同分异构体的结构简式CH2OHCH2COOH.
分析 5.4g水的物质的量为$\frac{5.4g}{18g/mol}$=0.3mol,n(H)=0.6 mol,13.2g二氧化碳的物质的量为$\frac{13.2g}{44g/mol}$=0.3mol,n(C)=n(CO2)=0.3 mol,此有机物9.0g含O元素质量:9.0g-0.6g-0.3×12 g=4.8 g,n(O)=$\frac{4.8g}{16g/mol}$=0.3 mol,故n(C):n(H):n(O)=0.3mol:0.6mol:0.3mol=1:2:1,即实验式为CH2O,设分子式为(CH2O)n,A的相对分子质量为90,可得30n=90,解得:n=3,故有机物A为C3H6O3,A分子的核磁共振氢谱有4个吸收峰,峰面积之比是1:1:1:3,应为CH3CH(OH)COOH,含有羧基和羟基,可发生酯化反应生成环酯或高聚物,以此解答该题.
解答 解:(1)5.4g水的物质的量为$\frac{5.4g}{18g/mol}$=0.3mol,n(H)=0.6 mol,13.2g二氧化碳的物质的量为$\frac{13.2g}{44g/mol}$=0.3mol,n(C)=n(CO2)=0.3 mol,此有机物9.0g含O元素质量:9.0g-0.6g-0.3×12 g=4.8 g,n(O)=$\frac{4.8g}{16g/mol}$=0.3 mol,故n(C):n(H):n(O)=0.3mol:0.6mol:0.3mol=1:2:1,即实验式为CH2O,设分子式为(CH2O)n,A的相对分子质量为90,可得30n=90,解得:n=3,故有机物A为C3H6O3;
故答案为:90;C3H6O3;
(2)A能与NaHCO3溶液发生反应,A一定含有羧基(-COOH);
故答案为:羧基;
(3)有机物A为C3H6O3,核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则分子中4种H原子的数目为1、1、1、3,分子中含有1个-COOH、1个-CH3、1个 CH、1个-OH,有机物A的结构简式为CH3CH(OH)COOH;
CH、1个-OH,有机物A的结构简式为CH3CH(OH)COOH;
故答案为:CH3CH(OH)COOH;
(4)CH3CH(OH)COOH反应得到含有六元环的酯类化合物的化学方程式是2CH3CH(OH)COOH $→_{△}^{浓硫酸}$ +2H2O,
+2H2O,
故答案为:2CH3CH(OH)COOH $→_{△}^{浓硫酸}$ +2H2O;
+2H2O;
(5)官能团与A相同的同分异构体的结构简式为CH2OHCH2COOH,故答案为:CH2OHCH2COOH.
点评 本题考查有机物的推断,侧重于学生的分析、计算能力的考查,题目涉及分子式与结构式的确定、官能团的性质等知识,题目难度中等,注意把握燃烧法及质量守恒确定有机物分子式的方法,明确常见有机物结构与性质.

 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案| A. | 最外层电子数:W>Z | B. | 气态氢化物的稳定性:X<Z | ||
| C. | 最高价氧化物对应水物的碱性:Y<W | D. | Y、Z的氧化物都是两性氧化物 |
| 目的 | 古代文献 | 说明 | |
| A | 使用 | “…凡研消(KNO3)不以铁碾入石臼,相激火生,祸不可测”-《天工开物》 | KNO3能自燃 |
| B | 性质 | “(火药)乃焰消(KNO3)、硫磺、山木炭所合,以为烽燧餇诸药者”-《本草纲目》 | 利用KNO3的氧化性 |
| C | 鉴别 | 区分硝石(KNO3)和朴消(Na2SO4):“以火烧之,紫青烟起,乃真硝石也”-《本草经集注》 | 利用焰色反应 |
| D | 提纯 | “…(KNO3)所在山泽,冬月地上有霜,扫取以水淋汁后,乃煎炼而成”-《开宝本草》 | 溶解、蒸发、结晶 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 火箭用偏二甲肼(C2H8N2)作燃料,N2O4作还原剂,反应产生巨大能量 | |
| B. | 铝制品由于表面有致密的氧化膜,可以稳定存在于空气中 | |
| C. | 硫是一种生命元素,自然界中的石膏矿、硫铁矿、赤铁矿等都是含“硫”为主的矿石 | |
| D. | 高纯度的SiO2对光有很好的折射和全反射作用,可以制成光电池将光能直接转化为电能 |
| A. | 最外层电子构型为ns2(n≠1),次外层电子数为8 | |
| B. | 外围电子构型为3d104s2 | |
| C. | 外围电子排布式为ns2np4 | |
| D. | 外围电子排布式为(n-1)d5ns2 |
| 选项 | 试剂甲 | 试剂乙 | 实验目的 |  |
| A | NaOH溶液 | 浓硫酸 | 从等体积NO、NH3和NO2中分离出NO | |
| B | KMnO4溶液 | 浓硫酸 | 除去Cl2中的SO2、HCl得干燥Cl2 | |
| C | 溴水 | 浓H2SO4 | 除去乙炔中的H2S和H2O(g) | |
| D | 品红溶液 | 石灰水 | 检验混合气体HCl、SO2、CO2中的SO2和CO2 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 水是无机物,故有机物在水中的溶解度都很小 | |
| B. | 氢键对物质的溶解性没有影响 | |
| C. | 溶质能与水发生化学反应将增大其在水中的溶解度 | |
| D. | CO与水都是极性分子,故CO易溶于水 |
 .
.