题目内容
“低碳循环”已引起各国家的高度重视,而如何降低大气中CO2的含量和有效地开发利用CO2正成为化学家研究的主要课题.
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
C+ KMnO4+ H2SO4→ CO2↑+ MnSO4+ K2SO4+ H2O
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:
①实验2条件下平衡常数K= .
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b的值 (填具体值或取值范围).
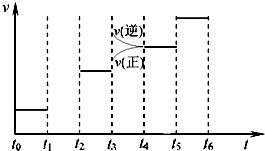
③实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时V正 V逆(选填“<”,
“>”或“=”).
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9.CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为1×10-4mol/L,则生成沉淀所需CaCl2溶液的最小浓度为 mol/L.
(4)最近科学家再次提出“绿色化学”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出,经化学反应后使空气中的CO2转变为可再生燃料甲醇.甲醇可制作燃料电池,写出以氢氧化钾为电解质甲醇燃料电池负极反应式 .当电子转移的物质的量为0.6mol时,参加反应的氧气的体积是 L(标准状况下).
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b的值
③实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时V正
“>”或“=”).
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9.CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为1×10-4mol/L,则生成沉淀所需CaCl2溶液的最小浓度为
(4)最近科学家再次提出“绿色化学”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出,经化学反应后使空气中的CO2转变为可再生燃料甲醇.甲醇可制作燃料电池,写出以氢氧化钾为电解质甲醇燃料电池负极反应式
考点:化学平衡常数的含义,化学电源新型电池,难溶电解质的溶解平衡及沉淀转化的本质
专题:化学平衡专题,电离平衡与溶液的pH专题,电化学专题
分析:(1)利用化合价升降法配平化学方程式;
(2)①先求得各物质平衡时的浓度,再根据平衡常数等于生成物浓度系数次幂之积除以反应物浓度系数次幂之积求得平衡常数;
②在反应中当反应物的物质的量之比等于化学计量数之比时,各反应物的转化率相等,某一种反应物越多,其转化率越低,而另一种反应物的转化率则越高,据此答题;
③根据浓度商Qc与平衡常数K的大小,判断反应进行的方向,进而确定正逆反应的速率;
(3)Na2CO3溶液的浓度为1×10-4mol/L,等体积混合后溶液中c(CO32-)=5.0×10-5mol/L,根据Ksp=c(CO32-)?c(Ca2+)计算沉淀时混合溶液中c(Ca2+),原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍;
(4)负极上燃料甲醇失电子发生氧化反应,正极上是氧气作氧化剂得电子发生还原反应,根据电极反应式可计算出氧气的体积.
(2)①先求得各物质平衡时的浓度,再根据平衡常数等于生成物浓度系数次幂之积除以反应物浓度系数次幂之积求得平衡常数;
②在反应中当反应物的物质的量之比等于化学计量数之比时,各反应物的转化率相等,某一种反应物越多,其转化率越低,而另一种反应物的转化率则越高,据此答题;
③根据浓度商Qc与平衡常数K的大小,判断反应进行的方向,进而确定正逆反应的速率;
(3)Na2CO3溶液的浓度为1×10-4mol/L,等体积混合后溶液中c(CO32-)=5.0×10-5mol/L,根据Ksp=c(CO32-)?c(Ca2+)计算沉淀时混合溶液中c(Ca2+),原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍;
(4)负极上燃料甲醇失电子发生氧化反应,正极上是氧气作氧化剂得电子发生还原反应,根据电极反应式可计算出氧气的体积.
解答:
解:(1)在反应中C从0价升到+4价,Mn元素从+7价降为+2价,利用化合价升降法及元素守恒配平化学方程式为5C+4KMnO4+6H2SO4=5CO2↑+4MnSO4+2K2SO4+6H2O,故答案为:5;4;6;5;4;2;6;
(2)①平衡时CO的物质的量为1.6mol,则:
CO(g)+H2O(g)?CO2(g)+H2(g),
开始(mol):2 1 0 0
变化(mol):0.4 0.4 0.4 0.4
平衡(mol):1.6 0.6 0.4 0.4
所以平衡常数K=
=
=0.17,故答案为:0.17;
②在反应中当反应物的物质的量之比等于化学计量数之比时,各反应物的转化率相等,某一种反应物越多,其转化率越低,而另一种反应物的转化率则越高,所以要使CO的转化率大于水蒸气,则0<
<1,故答案为:0<
<1;
③900℃时,当CO、H2O、CO2、H2均为1mol时,浓度商Qc=
=1>0.17=K,所以此时平衡要逆向移动,故V正<V逆,故答案为:<;
(3)Na2CO3溶液的浓度为1×10-4mol/L,等体积混合后溶液中c(CO32-)=5.0×10-5mol/L,根据Ksp=c(CO32-)?c(Ca2+)=2.8×10-9可知,c(Ca2+)=
mol/L=5.6×10-5mol/L,原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,故原溶液CaCl2溶液的最小浓度为2×5.6×10-5mol/L=1.12×10-4mol/L,故答案为:1.12×10-4;
(4)燃料电池中,负极上是燃料甲醇失电子发生氧化反应,在碱性环境下,电极反应式为:CH3OH+8OH?-6e-=CO32-+6H2O,正极上是氧气作氧化剂得电子发生还原反应,O2+2H2O+4e-=4OH?,转移0.6mol电子时,则参加反应的氧气的物质的量为0.15mol,其体积为0.15×22.4L=3.36L(标准状况下),
故答案为:CH3OH+8OH?-6e-=CO32-+6H2O;3.36.
(2)①平衡时CO的物质的量为1.6mol,则:
CO(g)+H2O(g)?CO2(g)+H2(g),
开始(mol):2 1 0 0
变化(mol):0.4 0.4 0.4 0.4
平衡(mol):1.6 0.6 0.4 0.4
所以平衡常数K=
| ||||
|
| 1 |
| 6 |
②在反应中当反应物的物质的量之比等于化学计量数之比时,各反应物的转化率相等,某一种反应物越多,其转化率越低,而另一种反应物的转化率则越高,所以要使CO的转化率大于水蒸气,则0<
| a |
| b |
| a |
| b |
③900℃时,当CO、H2O、CO2、H2均为1mol时,浓度商Qc=
| ||||
|
(3)Na2CO3溶液的浓度为1×10-4mol/L,等体积混合后溶液中c(CO32-)=5.0×10-5mol/L,根据Ksp=c(CO32-)?c(Ca2+)=2.8×10-9可知,c(Ca2+)=
| 2.8×10-9 |
| 5×10-5 |
(4)燃料电池中,负极上是燃料甲醇失电子发生氧化反应,在碱性环境下,电极反应式为:CH3OH+8OH?-6e-=CO32-+6H2O,正极上是氧气作氧化剂得电子发生还原反应,O2+2H2O+4e-=4OH?,转移0.6mol电子时,则参加反应的氧气的物质的量为0.15mol,其体积为0.15×22.4L=3.36L(标准状况下),
故答案为:CH3OH+8OH?-6e-=CO32-+6H2O;3.36.
点评:本题主要考查了氧化还原反应的配平、化学平衡常数的计算、转化率的应用、沉淀溶解的计算、电化学知识等知识点,综合性较强,中等难度,解题时注意对基础知识的灵活运用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列离子方程式正确的是( )
| A、碘化钾溶液跟适量溴水反应:I-+Br2═Br-+I2 |
| B、氯气与水的反应:Cl2+H2O═Cl-+ClO-+2H+ |
| C、二氧化锰与浓盐酸反应:MnO2+4H++2Cl-═Mn2++Cl2↑+2H2O |
| D、Cl2与氢氧化钠溶液的反应:Cl2+2 OH-═Cl-+ClO-+H2O |
 在盛有足量A的体积可变的密闭容器中通入B,发生反应:A(s)+2B(g)?4C(g)+D(g)△H>0,在一定温度、压强下达到平衡.平衡时C的物质的量与通入B的物质的量的变化关系如图所示.下列说法正确的是( )
在盛有足量A的体积可变的密闭容器中通入B,发生反应:A(s)+2B(g)?4C(g)+D(g)△H>0,在一定温度、压强下达到平衡.平衡时C的物质的量与通入B的物质的量的变化关系如图所示.下列说法正确的是( )| A、平衡时B的转化率为40% |
| B、若保持压强一定,当温度升高时,图中θ>45° |
| C、在容器中加入催化剂,则B的转化率增大 |
| D、若再通入B,则再次达平衡时C的体积分数增大 |
在天平的两个托盘上,放上质量相等的两个烧杯,在烧杯中分别加入等质量等浓度的硫酸,此时天平处于平衡状态,然后分别向两只烧杯中加入等质量的Na2CO3和NaHCO3粉末,完全反应后,则天平两边( )
| A、放Na2CO3的一端托盘下沉 |
| B、NaHCO3的一端托盘下沉 |
| C、仍保持平衡 |
| D、无法判断 |
下列说法不正确的是( )
| A、利用“地沟油”可制得肥皂 |
| B、含碳原子数不同的烷烃均互为同系物 |
| C、甲烷与氯气按照物质的量之比1:3充入试剂瓶中,光照充分反应后生成物为氯仿 (CHCl3)和HCl |
| D、CHCl2-CH3不可能为CH2=CH2的加成产物 |
下列说法错误的是( )
| A、H2O2溶液中加入MnO2或FeCl3溶液都能增大反应速率可用同一原理来解释 |
| B、已知FeS与某浓度的HNO3反应时生成Fe(NO3)3、H2SO4和某一单一的还原产物,若FeS和参与反应的HNO3的物质的量之比为1:6,则该反应的还原产物是NO |
| C、已知14 mol/L的H2SO4溶液的溶质质量分数为80%,那么7 mol/L的H2SO4溶液的溶质质量分数将大于40% |
| D、铁在少量氯气或过量的氯气中点燃所得产物不相同 |