题目内容
在天平的两个托盘上,放上质量相等的两个烧杯,在烧杯中分别加入等质量等浓度的硫酸,此时天平处于平衡状态,然后分别向两只烧杯中加入等质量的Na2CO3和NaHCO3粉末,完全反应后,则天平两边( )
| A、放Na2CO3的一端托盘下沉 |
| B、NaHCO3的一端托盘下沉 |
| C、仍保持平衡 |
| D、无法判断 |
考点:化学方程式的有关计算
专题:计算题
分析:在天平的两个托盘上,放上质量相等的两个烧杯,在烧杯中分别加入等质量等浓度的硫酸,此时天平处于平衡状态,然后分别向两只烧杯中加入等质量的Na2CO3和NaHCO3粉末,反应物放在一起不反应的状态时,天平是平衡的,指针的偏转主要是看生成二氧化碳的多少,因此解题时判断二氧化碳多少则成为解题的关键所在,所以可计算相同质量的Na2CO3和NaHCO3完全反应放出二氧化碳质量的大小,天平的指针会偏向质量大(下沉)的一方.
解答:
解:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,根据化学方程式,利用关系式法计算加入碳酸钠,溶液质量的变化.
Na2CO3~CO2↑ 溶液质量增加(△m)
106 44 62
106g 62g
2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑,根据化学方程式,利用关系式法计算加入碳酸氢钠,溶液质量的变化.
NaHCO3~CO2↑ 溶液质量增加(△m)
84 44 40
106g m
m=
=50.5g,所以加入碳酸钠一端溶液质量增重大,故放Na2CO3的一端托盘下沉,
故选:A.
Na2CO3~CO2↑ 溶液质量增加(△m)
106 44 62
106g 62g
2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑,根据化学方程式,利用关系式法计算加入碳酸氢钠,溶液质量的变化.
NaHCO3~CO2↑ 溶液质量增加(△m)
84 44 40
106g m
m=
| 106g×40 |
| 84 |
故选:A.
点评:本题是比较抽象的根据化学方程式的计算,解本题的关键是分析左右两盘实际质量的变化,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列反应中,属于吸热反应的是( )
| A、食物的腐败 |
| B、铝与稀盐酸反应 |
| C、二氧化碳与碳反应生成一氧化碳 |
| D、甲烷在氧气中的燃烧 |
下列叙述正确的是( )
| A、羊油是高分子化合物,是纯净物 |
| B、工业上将羊油加氢制造硬化油,有利于保存 |
| C、羊油是高级脂肪酸的高级醇酯 |
| D、羊油可以在碱性条件下加热水解制肥皂 |
化学与日常生活密切相关,下列说法正确的是( )
| A、碘酒只是指碘单质的乙醇溶液 |
| B、纯水不易导电,但属于电解质 |
| C、质量分数:医用酒精>生理盐水>食醋 |
| D、明矾可用于水的消毒、杀菌 |
有机化合物中的烯键跟臭氧(O3)反应,再在锌粉存在下水解,其结果是原有的烯键断裂,断裂处两端的碳原子各结合1个氧原子而生成醛基(-CHO)或酮基(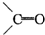 ),这两步反应合在一起,称为“烯键的臭氧化还原”,例如:(CH3)2═CHCH3
),这两步反应合在一起,称为“烯键的臭氧化还原”,例如:(CH3)2═CHCH3
(CH3)2C═O+CH3CH═O分子式为C4H8的几种烯烃混合气体经O3氧化并在锌粉存在下水解后生成0.60mol酮和1.80mol醛(其中HCHO 0.90mol)原混合气体中,2-丁烯的体积分数为( )
 ),这两步反应合在一起,称为“烯键的臭氧化还原”,例如:(CH3)2═CHCH3
),这两步反应合在一起,称为“烯键的臭氧化还原”,例如:(CH3)2═CHCH3| O3 |
| Zn、H2O |
| A、0.25 | B、0.33 |
| C、0.40 | D、0.50 |
为了更好的解决能源问题,人们一方面研究如何提高燃料的燃烧效率,另一方面寻找新能源.以下做法不能提高燃料效率的是( )
| A、煤的汽化与液化 |
| B、液体燃料呈雾状喷出 |
| C、将煤粉碎燃烧 |
| D、将煤压成煤球使用 |
塑料、合成橡胶和合成纤维这三大合成材料都是以煤、石油和天然气为原料生产的,下列有关说法错误的是( )
| A、天然气作为化工原料主要用于合成氨和生产甲醇 |
| B、煤可以直接液化,煤与氢气作用生成液体燃料 |
| C、乙烯、丙烯、甲烷等主要化工基本原料都可以由石油分馏得到 |
| D、聚乙烯塑料的主要成分聚乙烯是由乙烯通过加聚反应制得的 |