题目内容
在重水中存在下述电离平衡:D2O?D++OD-,因此,对重水(D2O)可采用pH一样的定义来规定pD,那么pD=-lg[D+].己知在某温度下D2O达电离平衡时,[D+]X[OD-]=1.6x 10 -15,则在下列叙述中:①用0.01mol NaOD和D2O配成1L溶液,其pD值等于2;②用0.01mol DCl溶于D2O中,配成1L溶液,其pD等于2;③纯净D2O在此温度下的pD大于7;④用 D2O配制0.2mol.L -I FeCl3溶液,溶液中Cl-浓度是Fe3+浓度的3倍.其中说法正确的组合是( )
| A、①② | B、①④ | C、③④ | D、②③ |
考点:水的电离
专题:电离平衡与溶液的pH专题
分析:①用0.01mol NaOD和D2O配成1L溶液,c(OD-)=0.01mol/L,c(D+)=
=1.6×10-13mol/L,其pD值等于12.8;
②用0.01mol DCl溶于D2O中,配成1L溶液,c(D+)=0.01mol/L,pD等于2;
③纯净D2O在此温度下,c(D+)=
=4×10-8mol/L,pD等于7.4,大于7;
④用 D2O配制0.2mol.L -I FeCl3溶液,Fe3+发生水解,故溶液中Cl-浓度大于Fe3+浓度的3倍.
| 1.6×10-15 |
| 0.01 |
②用0.01mol DCl溶于D2O中,配成1L溶液,c(D+)=0.01mol/L,pD等于2;
③纯净D2O在此温度下,c(D+)=
| 1.6×10-15 |
④用 D2O配制0.2mol.L -I FeCl3溶液,Fe3+发生水解,故溶液中Cl-浓度大于Fe3+浓度的3倍.
解答:
解:①用0.01mol NaOD和D2O配成1L溶液,c(OD-)=0.01mol/L,c(D+)=
=1.6×10-13mol/L,其pD值等于12.8,故①错误;
②用0.01mol DCl溶于D2O中,配成1L溶液,c(D+)=0.01mol/L,pD等于2,故②正确;
③纯净D2O在此温度下,c(D+)=
=4×10-8mol/L,pD等于7.4,大于7,故③正确;
④用 D2O配制0.2mol.L -I FeCl3溶液,Fe3+发生水解,故溶液中Cl-浓度大于Fe3+浓度的3倍,故④错误,
故说法正确的组合是②③,
故选D.
| 1.6×10-15 |
| 0.01 |
②用0.01mol DCl溶于D2O中,配成1L溶液,c(D+)=0.01mol/L,pD等于2,故②正确;
③纯净D2O在此温度下,c(D+)=
| 1.6×10-15 |
④用 D2O配制0.2mol.L -I FeCl3溶液,Fe3+发生水解,故溶液中Cl-浓度大于Fe3+浓度的3倍,故④错误,
故说法正确的组合是②③,
故选D.
点评:本题考查水的电离,难度中等.侧重学生知识迁移能力和信息运用能力的培养.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
A元素的阳离子与B元素的阴离子具有相同的电子层结构,有关两元素有以下叙述:①原子半径A<B ②离子半径A>B ③原子序数A>B ④原子最外层电子数A=B⑤A的正价与B的负价绝对值不一定相等.其中一定正确的是( )
| A、①② | B、③④⑤ | C、③⑤ | D、③④ |
塑料、合成橡胶和合成纤维这三大合成材料都是以煤、石油和天然气为原料生产的,下列有关说法错误的是( )
| A、天然气作为化工原料主要用于合成氨和生产甲醇 |
| B、煤可以直接液化,煤与氢气作用生成液体燃料 |
| C、乙烯、丙烯、甲烷等主要化工基本原料都可以由石油分馏得到 |
| D、聚乙烯塑料的主要成分聚乙烯是由乙烯通过加聚反应制得的 |
一定温度下,mg某物质A在足量氧气中充分燃烧,使燃烧产物跟足量过氧化钠反应,过氧化钠质量增加了ng,且n=m,以下符合此要求的物质有几个( )
①CH3OH ②C6H12O6 ③CH4 ④HCOOCH3⑤CH3CHO.
①CH3OH ②C6H12O6 ③CH4 ④HCOOCH3⑤CH3CHO.
| A、1 | B、2 | C、3 | D、4 |
将1mol乙醇(其中的氧用18O标记)在浓硫酸存在的条件下与1mol乙酸充分反应,下列叙述不正确的是( )
| A、生成的乙酸乙酯中含有18O |
| B、生成的水分中含有18O |
| C、可能生成88g乙酸乙酯 |
| D、不可能生成88g乙酸乙酯 |
化学与科学、技术、社会、环境密切相关.下列有关说法中错误的是( )
| A、节日燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 |
| B、小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂 |
| C、为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶 |
| D、面粉中禁止添加CaO2、过氧化苯甲酰等增白剂,CaO2属于过氧化物,过氧化苯甲酰属于有机物 |
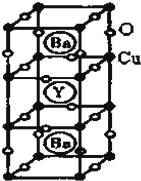 钇钡铜氧的晶胞结构如图.研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价.
钇钡铜氧的晶胞结构如图.研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价.