题目内容
 在盛有足量A的体积可变的密闭容器中通入B,发生反应:A(s)+2B(g)?4C(g)+D(g)△H>0,在一定温度、压强下达到平衡.平衡时C的物质的量与通入B的物质的量的变化关系如图所示.下列说法正确的是( )
在盛有足量A的体积可变的密闭容器中通入B,发生反应:A(s)+2B(g)?4C(g)+D(g)△H>0,在一定温度、压强下达到平衡.平衡时C的物质的量与通入B的物质的量的变化关系如图所示.下列说法正确的是( )| A、平衡时B的转化率为40% |
| B、若保持压强一定,当温度升高时,图中θ>45° |
| C、在容器中加入催化剂,则B的转化率增大 |
| D、若再通入B,则再次达平衡时C的体积分数增大 |
考点:化学平衡建立的过程,化学平衡的计算
专题:化学平衡专题
分析:根据在一定温度、压强下达到平衡,平衡时C的物质的量与加入B的物质的量的变化关系图可知,平衡时再加入B,因体积可变,则B的浓度不变,则平衡后B的加入平衡不移动;该反应是吸热反应,升高温度平衡正向移动,则C的物质的量增大;再由图可知,达平衡时B、C的物质的量相等来计算B的转化率,催化剂改变反应速率不改变化学平衡.
解答:
解:A、根据图象结合方程式知,加入的B物质的物质的量与生成C物质的物质的量相等,所以该反应中有一半的B物质反应,所以其转化率为50%,故A错误.
B、压强一定,当升高温度时,平衡正向移动,则C的物质的量增大,由图可以看出,图中θ>45°,故B正确;
C、在容器中加入催化剂,改变反应速率不改变化学平衡,则B的转化率不变,故C错误;
D、根据图象结合方程式知,加入的B物质的物质的量与生成C物质的物质的量相等,所以该反应中有一半的B物质反应,平衡时再加入B,因体积可变,则B的浓度不变,则平衡后B的加入平衡不移动,则再次达平衡时C的体积分数不变,故D错误;
故选B.
B、压强一定,当升高温度时,平衡正向移动,则C的物质的量增大,由图可以看出,图中θ>45°,故B正确;
C、在容器中加入催化剂,改变反应速率不改变化学平衡,则B的转化率不变,故C错误;
D、根据图象结合方程式知,加入的B物质的物质的量与生成C物质的物质的量相等,所以该反应中有一半的B物质反应,平衡时再加入B,因体积可变,则B的浓度不变,则平衡后B的加入平衡不移动,则再次达平衡时C的体积分数不变,故D错误;
故选B.
点评:本题考查化学平衡的图象分析,明确图象中的纵横坐标含有及隐含平衡时的信息是解答的关键,并利用影响化学反应速率及化学平衡的影响因素来解答,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
实验室需配制一种只含有四种离子(除H+和OH-外)的混合溶液,且在该混合溶液中四种离子的物质的量浓度均为0.1mol/L,以下各组能达到此目的是( )
| A、K+、SO42-、I-、NO3- |
| B、Cu2+、Na+、Cl-、S2- |
| C、Na+、K+、HCO3-、NO3- |
| D、K+、Ba2+、CH3COO-、Br- |
下列离子方程式正确的是( )
A、在稀氨水中通入过量CO2:NH3?H2O+CO2=NH
| ||||
| B、向碳酸氢钙溶液中加入过量氢氧化钠:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- | ||||
| C、向碳酸氢钙溶液中滴入过量澄清石灰水:Ca2++2HCO3-+2OH-→CaCO3↓+CO32-+2H2O | ||||
D、NH4HSO4溶液中加入足量Ba(OH)2溶液:H++SO
|
下列叙述正确的是( )
| A、羊油是高分子化合物,是纯净物 |
| B、工业上将羊油加氢制造硬化油,有利于保存 |
| C、羊油是高级脂肪酸的高级醇酯 |
| D、羊油可以在碱性条件下加热水解制肥皂 |
下列叙述正确的是( )
| A、氢氟酸不能保存在玻璃瓶内,也不和任何酸性氧化物反应 |
| B、实验室储存少量溴时,往往在液面上加少量水,防止溴被氧化 |
| C、氟化氢在空气中呈现白雾,这种白雾有剧毒 |
| D、碘化钾水溶液能使淀粉变蓝 |
化学与日常生活密切相关,下列说法正确的是( )
| A、碘酒只是指碘单质的乙醇溶液 |
| B、纯水不易导电,但属于电解质 |
| C、质量分数:医用酒精>生理盐水>食醋 |
| D、明矾可用于水的消毒、杀菌 |
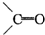 ),这两步反应合在一起,称为“烯键的臭氧化还原”,例如:(CH3)2═CHCH3
),这两步反应合在一起,称为“烯键的臭氧化还原”,例如:(CH3)2═CHCH3