题目内容
设NA代表阿伏加德罗常数.下列有关叙述正确的是( )
| A、分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28g |
| B、常温下,1L0.1mol.L-1的NH4NO3溶液中NH4+和NO3-总数为0.2NA |
| C、标准状况下,4.48 L重水(D20)含有的中子数为2NA |
| D、1 mol甲基(-CH3)所含电子数为9NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.没有告诉在标准状况下,不能使用标况下的气体摩尔体积计算;
B.铵根离子部分水解,溶液中铵根离子的数目减少;
C.重水在标况下不是气体,不能使用气体摩尔体积计算;
D.甲基中含有9个电子,1mol甲基中含有9mol电子.
B.铵根离子部分水解,溶液中铵根离子的数目减少;
C.重水在标况下不是气体,不能使用气体摩尔体积计算;
D.甲基中含有9个电子,1mol甲基中含有9mol电子.
解答:
解:A.不是标准状况下,不能用22.4L/mol计算气体的体积,故A错误;
B.1L 0.1mol.L-1的NH4NO3溶液中含有溶质硝酸铵0.1mol,由于铵根离子部分水解,则NH4+和NO3-总物质的量小于0.2mol,NH4+和NO3-的整数小于0.2NA,故B错误;
C.标况下重水不是气体,不能使用标况下的气体摩尔体积计算重水的物质的量,故C错误;
D.甲基为中性原子团,每个甲基中含有9个电子,1mol甲基中含有9mol电子,所含电子数为9NA,故D正确;
故选D.
B.1L 0.1mol.L-1的NH4NO3溶液中含有溶质硝酸铵0.1mol,由于铵根离子部分水解,则NH4+和NO3-总物质的量小于0.2mol,NH4+和NO3-的整数小于0.2NA,故B错误;
C.标况下重水不是气体,不能使用标况下的气体摩尔体积计算重水的物质的量,故C错误;
D.甲基为中性原子团,每个甲基中含有9个电子,1mol甲基中含有9mol电子,所含电子数为9NA,故D正确;
故选D.
点评:本题考查阿伏伽德罗常数的综合应用,题目难度中等,试题侧重考查标况下气体摩尔体积的使用条件、盐的水解原理,注意掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间关系,明确羟基与氢氧根离子、甲基与甲烷的区别.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
将1mol SO2和1mol O2通入体积不变的密闭容器中,在一定条件下发生反应2SO2(g)+O2(g)
2SO3(g),达到平衡时SO3 为0.3mol,此时若移走0.5mol O2和0.5mol SO2,相同温度下再次达到新平衡时SO3的物质的量为( )
| 催化剂 |
| △ |
| A、0.3mol |
| B、0.15mol |
| C、小于0.15mol |
| D、大于0.15mol,小于0.3mol |
化学与科技、社会、生产、生活等关系密切,下列有关说法不正确的是( )
| A、部分卤代烃可用作灭火剂 |
| B、石油分馏是物理变化,可得到的产品有汽油、煤油和柴油 |
| C、提倡人们购物时不用塑料袋,是为了防止白色污染 |
| D、35%-40%甲醛溶液俗称为福尔马林,可用来浸泡海产品来起到保鲜效果 |

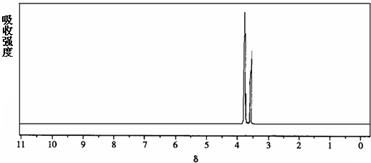
 实验室用中和滴定法测定待测烧碱溶液的浓度,试根据实验回答:
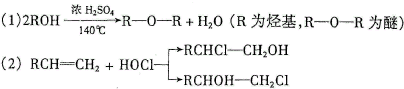
实验室用中和滴定法测定待测烧碱溶液的浓度,试根据实验回答: )的化合物反应生成醇,其过程可表示如下:
)的化合物反应生成醇,其过程可表示如下: (-R1、-R2表示烃基)
(-R1、-R2表示烃基)

