题目内容
镍是一种十分重要的有色金属,但粗镍中一般含有Fe、Cu及难与酸、碱溶液反应的不溶性杂质而影响使用.现对粗镍进行提纯,具体的反应流程如下:

已知:
①2Ni2O3(黑色)
4NiO(暗绿色)+O2↑
②
根据信息回答:
(1)28Ni在周期表中的第 周期;镍与稀硝酸反应的离子方程式为 .实验表明镍的浸出率与温度有关,随着温度升高镍的浸出率增大,但当温度高于70℃时,镍的浸出率又降低,浸出渣中Ni(OH)2含量增大,其原因为 ;
(2)在溶液A的净化除杂中,首先将溶液A煮沸,调节PH=5.5,加热煮沸5min,静置一段时间后,过滤出Fe(OH)3.为了得到纯净的溶液B还需要加入以下物质 进行除杂(填正确答案标号).
A、NaOH B、Na2S C、H2S D、NH3?H2O
(3)已知以下三种物质的溶解度关系:NiC2O4>NiC2O4?H2O>NiC2O4?2H2O.则操作Ⅰ、Ⅱ名称是 、 ; D生成E的化学方程式为 .
(4)1molE经上述流程得到纯镍,理论上参加反应的氢气为 mol.
(5)测定样品中的镍含量的基本思路是将Ni2+转化为沉淀,通过测量沉淀的质量进一步推算Ni含量.已知Ni2+能与CO32-,C2O42-、S2-等离子形成沉淀,但测定时常选用丁二酮肟(C4H8N2O2)作沉淀剂,生成分子式为C8H14N4O4Ni的鲜红色沉淀.从实验误差角度分析主要原因为: .

已知:
①2Ni2O3(黑色)
| ||
②
| 物质 | CuS | Cu(OH)2 | Ni(OH)2 | NiS |
| Ksp | 8.8×10-36 | 2.2×10-20 | 5.48×10-16 | 3.2×10-19 |
(1)28Ni在周期表中的第
(2)在溶液A的净化除杂中,首先将溶液A煮沸,调节PH=5.5,加热煮沸5min,静置一段时间后,过滤出Fe(OH)3.为了得到纯净的溶液B还需要加入以下物质
A、NaOH B、Na2S C、H2S D、NH3?H2O
(3)已知以下三种物质的溶解度关系:NiC2O4>NiC2O4?H2O>NiC2O4?2H2O.则操作Ⅰ、Ⅱ名称是
(4)1molE经上述流程得到纯镍,理论上参加反应的氢气为
(5)测定样品中的镍含量的基本思路是将Ni2+转化为沉淀,通过测量沉淀的质量进一步推算Ni含量.已知Ni2+能与CO32-,C2O42-、S2-等离子形成沉淀,但测定时常选用丁二酮肟(C4H8N2O2)作沉淀剂,生成分子式为C8H14N4O4Ni的鲜红色沉淀.从实验误差角度分析主要原因为:
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:流程分析可知,粗镍稀硫酸酸溶得到溶液A含有Ni2+、Fe3+、Cu2+,净化除杂得到溶液B加入草酸溶液充分反应得到浊液C过滤经过调节溶液PH沉淀镍离子,洗涤干燥得到NiC2O4?2H2O,空气中加热分解生成Ni2O3,加热反应生成暗红色NiO用氢气还原得到镍;
(1)28Ni核外有4层电子,是第四周期元素;根据流程图可知镍与稀硝酸反应生成硝酸镍和NO、水,Ni(OH)2是由Ni2+水解而得到的,所以温度过高时Ni2+的水解程度变大,浸出渣中Ni(OH)2含量增大;
(2)AB选项中含有Na+,则溶液B中有Na+杂质,不纯净,错误;若选用D,则Cu(OH)2 Ni(OH)2的溶度积相差不大,而且引入NH4+,不易的纯净的硝酸镍溶液,错误;C、CuS与NiS的溶度积相差很大,Cu2+沉淀完全而且不会引入新的杂质,正确,答案选C;
(3)利用3种物质的溶解度的差异,浊液C中主要得NiC2O4?2H2O,所以沉淀过滤之后应洗涤、干燥沉淀;固体E为黑色,所以应是Ni2O3;则D生成E的化学方程式为4NiC2O4?2H2O+3 O2=2Ni2O3+8CO2↑+8H2O;
(4)1mol Ni2O3经上述流程转化为2molNiO,2molNiO与氢气发生氧化还原反应,生成单质镍,需要氢气的物质的量是2mol;
(5)因为Ni2+与丁二酮肟(C4H8N2O2)生成的C8H14N4O4Ni鲜红色沉淀的沉淀质量大,称量误差小,分析结果准确度高.
(1)28Ni核外有4层电子,是第四周期元素;根据流程图可知镍与稀硝酸反应生成硝酸镍和NO、水,Ni(OH)2是由Ni2+水解而得到的,所以温度过高时Ni2+的水解程度变大,浸出渣中Ni(OH)2含量增大;
(2)AB选项中含有Na+,则溶液B中有Na+杂质,不纯净,错误;若选用D,则Cu(OH)2 Ni(OH)2的溶度积相差不大,而且引入NH4+,不易的纯净的硝酸镍溶液,错误;C、CuS与NiS的溶度积相差很大,Cu2+沉淀完全而且不会引入新的杂质,正确,答案选C;
(3)利用3种物质的溶解度的差异,浊液C中主要得NiC2O4?2H2O,所以沉淀过滤之后应洗涤、干燥沉淀;固体E为黑色,所以应是Ni2O3;则D生成E的化学方程式为4NiC2O4?2H2O+3 O2=2Ni2O3+8CO2↑+8H2O;
(4)1mol Ni2O3经上述流程转化为2molNiO,2molNiO与氢气发生氧化还原反应,生成单质镍,需要氢气的物质的量是2mol;
(5)因为Ni2+与丁二酮肟(C4H8N2O2)生成的C8H14N4O4Ni鲜红色沉淀的沉淀质量大,称量误差小,分析结果准确度高.
解答:
解:(1)28Ni核外有4层电子,是第四周期元素;根据流程图可知镍与稀硝酸反应生成硝酸镍和NO、水,离子方程式为:3Ni+8H++2NO3-=3Ni2++2NO↑+4H2O;实验表明镍的浸出率与温度有关,随着温度升高镍的浸出率增大,但当温度高于70℃时,镍的浸出率又降低,浸出渣中Ni(OH)2含量增大,Ni(OH)2是由Ni2+水解而得到的,所以温度过高时Ni2+的水解程度变大,浸出渣中Ni(OH)2含量增大;
故答案为:四,3Ni+8H++2NO3-=3Ni2++2NO↑+4H2O;温度升高时,Ni2+ 的水解程度变大;
(2)AB选项中含有Na+,则溶液B中有Na+杂质,不纯净,错误;若选用D,则Cu(OH)2 Ni(OH)2的溶度积相差不大,而且引入NH4+,不易的纯净的硝酸镍溶液,错误;C、CuS与NiS的溶度积相差很大,Cu2+沉淀完全而且不会引入新的杂质,正确,
故答案为:C;
(3)利用3种物质的溶解度的差异,浊液C中主要得NiC2O4?2H2O,所以沉淀过滤之后应洗涤、干燥沉淀,则操作Ⅰ、Ⅱ名称是洗涤、干燥;固体E为黑色,所以应是Ni2O3;则D生成E的化学方程式为:4NiC2O4?2H2O+3 O2=2Ni2O3+8CO2↑+8H2O;
故答案为:洗涤,干燥,4NiC2O4?2H2O+3O2=2Ni2O3+8CO2↑+8H2O;
(4)1mol Ni2O3经上述流程转化为2molNiO,2molNiO与氢气发生氧化还原反应,生成单质镍,需要氢气的物质的量是2mol;
故答案为:2;
(5)因为Ni2+与丁二酮肟(C4H8N2O2)生成的C8H14N4O4Ni鲜红色沉淀的沉淀质量大,称量误差小,分析结果准确度高.
故答案为:生成沉淀质量大,称量误差小,分析结果准确度高.
故答案为:四,3Ni+8H++2NO3-=3Ni2++2NO↑+4H2O;温度升高时,Ni2+ 的水解程度变大;
(2)AB选项中含有Na+,则溶液B中有Na+杂质,不纯净,错误;若选用D,则Cu(OH)2 Ni(OH)2的溶度积相差不大,而且引入NH4+,不易的纯净的硝酸镍溶液,错误;C、CuS与NiS的溶度积相差很大,Cu2+沉淀完全而且不会引入新的杂质,正确,
故答案为:C;
(3)利用3种物质的溶解度的差异,浊液C中主要得NiC2O4?2H2O,所以沉淀过滤之后应洗涤、干燥沉淀,则操作Ⅰ、Ⅱ名称是洗涤、干燥;固体E为黑色,所以应是Ni2O3;则D生成E的化学方程式为:4NiC2O4?2H2O+3 O2=2Ni2O3+8CO2↑+8H2O;
故答案为:洗涤,干燥,4NiC2O4?2H2O+3O2=2Ni2O3+8CO2↑+8H2O;
(4)1mol Ni2O3经上述流程转化为2molNiO,2molNiO与氢气发生氧化还原反应,生成单质镍,需要氢气的物质的量是2mol;
故答案为:2;
(5)因为Ni2+与丁二酮肟(C4H8N2O2)生成的C8H14N4O4Ni鲜红色沉淀的沉淀质量大,称量误差小,分析结果准确度高.
故答案为:生成沉淀质量大,称量误差小,分析结果准确度高.
点评:本题考查了物质分离方法和流程的理解应用,主要是物质性质分析,反应离子方程式书写,除杂方法的应用,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
下列化学用语的表达或使用正确的是( )
A、氟离子的结构示意图: |
B、CH4的比例模型: |
C、羧基的电子式: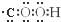 |
| D、NaHCO3的电离方程式:NaHCO3═Na++H++CO32- |
将表面已完全钝化的铝条,插入下列溶液中,不会发生反应的是( )
| A、稀硝酸 | B、稀盐酸 |
| C、硝酸铜 | D、氢氧化钠 |

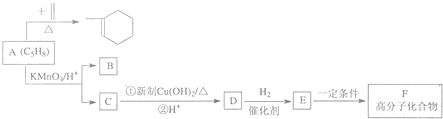
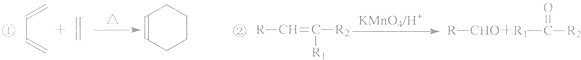
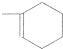 时,A发生的反应类型为
时,A发生的反应类型为
