题目内容
已知某烃分子中碳元素的质量分数为82.76%,在标准状况下它的密度为2.59g/L.
则:(1)此有机物的相对分子质量为 ;
(2)此有机物的分子式为 ;
(3)若该有机物分子结构中含有2个甲基,其结构简式为 .
则:(1)此有机物的相对分子质量为
(2)此有机物的分子式为
(3)若该有机物分子结构中含有2个甲基,其结构简式为
考点:有机物实验式和分子式的确定
专题:有机物分子组成通式的应用规律
分析:根据烷烃的摩尔质量M=ρVm求出相对摩尔质量,利用摩尔质量和相对分子质量在数值上相等,求出相对分子质量,根据含碳量可计算含氢量,进而计算分子中碳、氢原子的个数,由此写出有机物的分子式.
解答:
解:某烃的摩尔质量M=2.59g/L×22.4L/mol=58g/mol,即相对分子质量为58,
1mol 某烃中含C:
═4;
1mol 某烃中含H:
═10
故某烃的分子式为:C4H10,
若该有机物分子结构中含有2个甲基,其结构简式为CH3CH2CH2CH3;
故答案为:(1)58 (2)C4H10(3)CH3CH2 CH2 CH3.
1mol 某烃中含C:
| 58×82.76% |
| 12 |
1mol 某烃中含H:
| 58(1-82.76%) |
| 1 |
故某烃的分子式为:C4H10,
若该有机物分子结构中含有2个甲基,其结构简式为CH3CH2CH2CH3;
故答案为:(1)58 (2)C4H10(3)CH3CH2 CH2 CH3.
点评:本题考察了有机物分子式的推断,难度中等,要求学生掌握同温同压下气体的摩尔质量与密度关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列变化过程中,共价键被破坏的是 ( )
| A、烧碱固体溶于水 |
| B、氯化氢气体溶于水 |
| C、二氧化碳变成干冰 |
| D、碘溶于酒精 |
 一些简单原子的原子结构可用如图①、②、③形象地表示:根据该图的示意,则下列有关图①、②、③所表示的原子叙述正确的是( )
一些简单原子的原子结构可用如图①、②、③形象地表示:根据该图的示意,则下列有关图①、②、③所表示的原子叙述正确的是( )| A、①②③互为同位素 |
| B、①②③互为同素异形体 |
| C、①②③为同种原子 |
| D、①②③具有相同的质量数 |
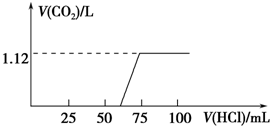 某化学兴趣小组同学用实验室中一瓶久置的NaOH固体做了以下实验:先称取13.3g NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入浓度为4mol?L-1的盐酸,再根据生成的CO2体积计算出Na2CO3质量,从而进一步计算出样品中变质NaOH的质量.实验测得加入盐酸的体积与产生CO2的体积(标况)关系如图所示:
某化学兴趣小组同学用实验室中一瓶久置的NaOH固体做了以下实验:先称取13.3g NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入浓度为4mol?L-1的盐酸,再根据生成的CO2体积计算出Na2CO3质量,从而进一步计算出样品中变质NaOH的质量.实验测得加入盐酸的体积与产生CO2的体积(标况)关系如图所示: