题目内容
下列有关的离子方程式正确的是( )
| A、向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ | ||||
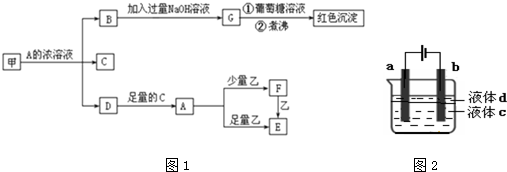
B、铜片接电源正极,碳棒接电源负极,电解硫酸铜溶液:Cu+2H+
| ||||
| C、在100mL浓度为1mol?L-1的Fe(NO3)3的溶液中通入足量SO2 2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | ||||
| D、实验室配制的亚铁盐溶液在空气中被氧化:4Fe2++O2+2H2O═4Fe3++4OH- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.氢氧化铁比氢氧化镁更难溶,氢氧化镁与氯化铁反应生成氢氧化铁和镁离子;
B.电解过程中,溶液中水电离的氢离子放电生成氢气,同时生成氢氧根离子,氢氧根离子与铜离子反应生成氢氧化铜沉淀;
C.二氧化硫足量,硝酸根离子在酸性条件下氧化性大于铁离子,硝酸根离子优先反应,反应产物中没有亚铁离子生成;
D.氢氧根离子能够与铁离子反应生成氢氧化铁沉淀.
B.电解过程中,溶液中水电离的氢离子放电生成氢气,同时生成氢氧根离子,氢氧根离子与铜离子反应生成氢氧化铜沉淀;
C.二氧化硫足量,硝酸根离子在酸性条件下氧化性大于铁离子,硝酸根离子优先反应,反应产物中没有亚铁离子生成;
D.氢氧根离子能够与铁离子反应生成氢氧化铁沉淀.
解答:
解:A.向FeCl3溶液中加入Mg(OH)2,氢氧化镁沉淀转化成氢氧化铁沉淀,反应的离子方程式为:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+,故A正确;
B.铜片接电源正极,碳棒接电源负极,电解硫酸铜溶液,反应生成氢氧化铜沉淀,正确的离子方程式为:Cu+2H2O
Cu(OH)2↓+H2↑,故B错误;
C.在100mL浓度为1mol?L-1的Fe(NO3)3的溶液中通入足量SO2,硝酸根离子在酸性条件下的氧化性大于铁离子,二氧化硫足量,铁离子不参与反应,正确的离子方程式为:2NO3-+3SO2+2H2O═2NO↑+3SO42-+4H+,故C错误;
D.亚铁盐溶液在空气中被氧化生成氢氧化铁沉淀和铁离子,正确的离子方程式为:12Fe2++3O2+6H2O═8Fe3++4Fe(OH)3↓,故D错误;
故选A.
B.铜片接电源正极,碳棒接电源负极,电解硫酸铜溶液,反应生成氢氧化铜沉淀,正确的离子方程式为:Cu+2H2O
| ||
C.在100mL浓度为1mol?L-1的Fe(NO3)3的溶液中通入足量SO2,硝酸根离子在酸性条件下的氧化性大于铁离子,二氧化硫足量,铁离子不参与反应,正确的离子方程式为:2NO3-+3SO2+2H2O═2NO↑+3SO42-+4H+,故C错误;
D.亚铁盐溶液在空气中被氧化生成氢氧化铁沉淀和铁离子,正确的离子方程式为:12Fe2++3O2+6H2O═8Fe3++4Fe(OH)3↓,故D错误;
故选A.
点评:本题考查了离子方程式的正误判断,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等),选项CD为难点、易错点,注意正确判断反应物、生成物.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案
相关题目
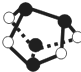 NA表示阿伏加德罗常数的值,下列说法正确的是( )
NA表示阿伏加德罗常数的值,下列说法正确的是( )| A、0.5mol雄黄(As4S4结构如图)含有NA个S-S键 | ||||
| B、7.8g Na2S和7.8g Na2O2中含有的阴离子数目均为0.1NA | ||||
C、1.8g
| ||||
| D、氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24L |
下列实验操作或装置符合实验要求的是( )


| A、装置Ⅰ可用于测定中和热 |
| B、装置Ⅱ装置放置一段时间后,饱和CuSO4溶液中不出现蓝色晶体 |
| C、装置Ⅲ中的石英坩埚可用于熔化氢氧化钠 |
| D、装置Ⅳ可用于吸收易溶于水的尾气 |
下列化学反应对应的离子方程式表示正确的是( )
| A、FeCl3溶液与Cu的反应:Cu+Fe3+═Cu2++Fe2+ |
| B、NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O |
| C、少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O═C6H5OH+HSO3- |
| D、FeBr2溶液与等物质的量的Cl2反应:2Fe2++2Br-+2Cl2═2Fe3++4Cl-+Br2 |
某有机物M的结构简式如图所示,下列有关叙述正确的是( )


| A、1mol M最多可以与2mol Br2发生反应 |
| B、M在一定条件下可以发生消去反应、取代反应和加成反应 |
| C、一个M分子中最多有8个碳原子在同一平面上 |
| D、1mol M与足量的NaOH溶液反应,最多可以消耗3mol NaOH |
某一元弱酸HA的相对分子质量为M.在t℃时,将a gHA完全溶解于水,得VmL饱和溶液,测得该溶液的密度为ρg?cm-3,其中n(A-)为bmol.下列叙述,错误的是( )
A、溶液中c(H+)=
| ||
B、物质的量浓度c(HA)=
| ||
C、t℃时,HA的溶解度S=
| ||
D、HA的质量分数w(HA)=
|
NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、84g NaHCO3晶体中含有NA个CO32- |
| B、0.1mol?L-1K2CO3溶液中,阴离子总数大于0.1NA |
| C、1.8g石墨和C60的混合物中,碳原子数目为0.15NA |
| D、标准状况下,22.4L CCl4中含有的共用电子对数目为4NA |